മാക്യുലാർ ഡീജനറേഷൻ
| മാക്യുലാർ ഡീജനറേഷൻ | |
|---|---|
| മറ്റ് പേരുകൾ | പ്രായവുമായിബന്ധപ്പെട്ട മാക്യുലാർ ഡീജനറേഷൻ |
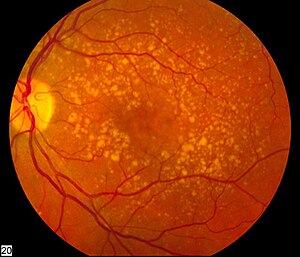 | |
| ഇന്റർമീഡിയറ്റ് മാക്യുലാർ ഡീജനറേഷൻ കാണിക്കുന്ന റെറ്റിന ചിത്രം | |
| സ്പെഷ്യാലിറ്റി | നേത്ര വിജ്ഞാനം |
| ലക്ഷണങ്ങൾ | കാഴ്ച മണ്ഡലത്തിന്റെ മധ്യ ഭാഗത്തുള്ള മങ്ങിയ കാഴ്ച or കാഴ്ച നഷ്ടം[1] |
| സങ്കീർണത | വിഷ്വൽ ഹാലൂസിനേഷൻ[1] |
| സാധാരണ തുടക്കം | പ്രായാധിക്യം[1] |
| തരങ്ങൾ | ഏർളി, ഇന്റർമീഡിയറ്റ്, ലേറ്റ്[1] |
| കാരണങ്ങൾ | റെറ്റിനയിലെ മാക്യുലയ്ക്ക് ഉണ്ടാകുന്ന തകരാറ്[1] |
| അപകടസാധ്യത ഘടകങ്ങൾ | ജനിതകം, പുകവലി[1] |
| ഡയഗ്നോസ്റ്റിക് രീതി | നേത്ര പരിശോധന[1] |
| പ്രതിരോധം | വ്യായാമം, ആരോഗ്യകരമായ ഭക്ഷണ ശീലങ്ങൾ, പുകവലി ഒഴിവാക്കുക[1] |
| Treatment | കണ്ണിലേക്ക് കുത്തിവെക്കുന്നആന്റി വിഇജി എഫ് മരുന്നുകൾ, ലേസർ കൊയാഗുലേഷൻ, ഫോട്ടോഡൈനാമിക് തെറാപ്പി[1] |
| ആവൃത്തി | 6.2 മില്യൺ (2015)[2] |
ദൃശ്യ മണ്ഡലത്തിൻ്റെ അതായത് വിഷ്വൽ ഫീൽഡിന്റെ മധ്യഭാഗത്തെ കാഴ്ച നഷ്ടപ്പെടുന്ന ഒരു മെഡിക്കൽ അവസ്ഥയാണ് മാക്യുലാർ ഡീജനറേഷൻ. ഇത് പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലാർ ഡീജനറേഷൻ (എഎംഡി /എആർഎംഡി) എന്നും അറിയപ്പെടുന്നു.[1] ഈ അസുഖത്തിന് തുടക്കത്തിൽ പലപ്പോഴും ലക്ഷണങ്ങളൊന്നും ഉണ്ടാകില്ല. എന്നാൽ കാലക്രമേണ, ഒരു കണ്ണിലെയോ രണ്ട് കണ്ണിലെയോ കാഴ്ച കുറഞ്ഞു വരുന്നു. ഇത് സാധാരണയായി പൂർണ്ണമായ അന്ധതയ്ക്ക് കാരണമാകുന്ന രോഗം അല്ലെങ്കിലും, കേന്ദ്ര കാഴ്ച നഷ്ടപ്പെടുന്നത് മൂലം മുഖങ്ങൾ തിരിച്ചറിയാനോ, ഡ്രൈവ് ചെയ്യാനോ, വായിക്കാനോ, ദൈനംദിന ജീവിതത്തിലെ മറ്റ് പ്രവർത്തനങ്ങൾ നടത്തുന്നതിനോ ഒക്കെ പ്രയാസം ഉണ്ടാക്കിയേക്കാം. മാക്യുലർ ഡീജനറേഷൻ വന്നവരിൽ ചിലപ്പോൾ വിഷ്വൽ ഹാലൂസിനേഷൻ സംഭവിക്കാം, പക്ഷേ ഇവ ഒരു മാനസികരോഗത്തെ പ്രതിനിധീകരിക്കുന്നില്ല.
പ്രായമായവരിൽ ആണ് മാക്യുലർ ഡീജനറേഷൻ സാധാരണ സംഭവിക്കാറുള്ളത്.[1] ജനിതക ഘടകങ്ങളും, പുകവലിയും ഇതിൽ ഒരു പങ്കു വഹിക്കുന്നു. റെറ്റിനയുടെ മാക്യുലയ്ക്ക് കേടുപാടുകൾ സംഭവിക്കുന്നതാണ് ഇതിന് കാരണം. പൂർണ്ണമായ നേത്ര പരിശോധനയിലൂടെ രോഗനിർണ്ണയം സാധ്യമാണ്. തീവ്രതയ്ക്കനുസരിച്ച് ഈ രോഗം 'ഏർളി', 'ഇന്റർമീഡിയറ്റ്', 'ലേറ്റ്' എന്നിങ്ങനെ മൂന്നായി തരം തിരിച്ചിരിക്കുന്നു. ലേറ്റ് മാക്യുലർ ഡീജനറേഷൻ "ഡ്രൈ", "വെറ്റ്" രൂപങ്ങളായി വീണ്ടും വിഭജിക്കപ്പെട്ടിട്ടുണ്ട്. ഡ്രൈ വിഭാഗത്തിൽ ആണ് 90% കേസുകളും ഉൾപ്പെടുന്നത്.[3]
വ്യായാമം, പോഷക സമൃദ്ധമായ ഭക്ഷണം കഴിക്കുക, പുകവലി ഒഴിവാക്കുക എന്നിങ്ങനെയുള്ള കാര്യങ്ങൾ ഈ രോഗത്തെ പ്രതിരോധിക്കാറുണ്ട്.[1] പക്ഷെ ഇതു മൂലം നഷ്ടപ്പെട്ട കാഴ്ചയെ തിരികെ നൽകുന്ന ഒരു ചികിത്സ നിലവിൽ ഇല്ല. വെറ്റ് രോഗാവസ്ഥയിൽ, കണ്ണിലേക്ക് കുത്തിവയ്ക്കുന്ന ആന്റി-വിഇജിഎഫ് മരുന്നുകൾ അല്ലെങ്കിൽ ലേസർ കൊയാഗ്യുലേഷൻ, ഫോട്ടോഡൈനാമിക് തെറാപ്പി എന്നീ ചികിൽസാരീതികൾ കാഴ്ച വീണ്ടും മോശമാകുന്ന തോത് മന്ദഗതിയിലാക്കാം. ആന്റിഓക്സിഡൻ്റുകളും, വിറ്റാമിനുകളും, ധാതുക്കളും രോഗ പ്രതിരോധത്തിന് ഉപയോഗപ്രദമാണെന്ന് പറയുന്നില്ല.[4] എന്നിരുന്നാലും, ഡയറ്ററി സപ്ലിമെൻറുകൾ ഇതിനകം രോഗം ഉള്ളവരിൽ രോഗ പുരോഗതിയെ മന്ദഗതിയിലാക്കിയേക്കാം. [5]
2015 ൽ ഇത് ആഗോളതലത്തിൽ 6.2 ദശലക്ഷം ആളുകളെ ബാധിച്ചു എന്നാണ് കണക്കായിരിക്കുന്നത്.[2] 2013 ലെ കണക്ക് പ്രകാരം തിമിരം, മാസം തികയാതെയുള്ള ജനനം, ഗ്ലോക്കോമ എന്നിവയ്ക്ക് ശേഷമുള്ള അന്ധതയുടെ ഏറ്റവും സാധാരണമായ നാലാമത്തെ കാരണമാണ് ഇത്.[6] ഇത് സാധാരണയായി അമ്പത് വയസ്സിനു മുകളിലുള്ളവരെയാണ് ബാധിക്കുന്നത്, അമേരിക്കയിൽ ഈ പ്രായത്തിലുള്ളവരിലെ കാഴ്ച നഷ്ടത്തിൻറെ ഏറ്റവും സാധാരണ കാരണം ഇതാണ്.[1] [3] 50 നും 60 നും ഇടയിൽ പ്രായമുള്ളവരിൽ 0.4% പേർക്ക് ഈ രോഗം ഉണ്ട്, അതേസമയം 60 മുതൽ 70 വരെ ആളുകളിൽ 0.7%, ആളുകൾക്ക് 70 നും 80 നും ഇടയിൽ 2.3% ആളുകൾക്ക്, 80 വയസ്സിനു മുകളിലുള്ള വരിൽ 12% എന്നിങ്ങനെ ഇത് സംഭവിക്കുന്നു.
അടയാളങ്ങളും ലക്ഷണങ്ങളും[തിരുത്തുക]


മാക്യുലർ ഡീജനറേഷന്റെ ലക്ഷണങ്ങളും അടയാളങ്ങളും താഴെ പറയുന്നവയാണ്:
- ദൃശ്യ ലക്ഷണങ്ങൾ
- വികലമായ കാഴ്ചയുടെ രൂപത്തിൽ വരുന്ന മെറ്റാമോർഫോപ്സിയ, അതിൽ നേർരേഖകളുടെ ഒരു ഗ്രിഡ് വളഞ്ഞതുപോലെ കാണപ്പെടുകയും ഗ്രിഡിന്റെ ചില ഭാഗങ്ങൾ ശൂന്യമായി കാണപ്പെടുകയും ചെയ്യും: ഡ്രൈവിംഗ് സമയത്ത് വീട്ടിലെ മിനിബ്ലൈൻഡുകളോ ടെലിഫോൺ പോളുകളോ പോലുള്ള കാര്യങ്ങൾ നോക്കുമ്പോൾ രോഗികൾ ആദ്യം ഇത് ശ്രദ്ധിക്കാറുണ്ട്. ഇതോടൊപ്പം സെൻട്രൽ സ്കോട്ടോമകൾ, ഷാഡോകൾ എന്നിവയും ഉണ്ടാകാം.
- ശോഭയുള്ള പ്രകാശത്തിലേക്ക് നോക്കിയ ശേഷം കാഴ്ച വീണ്ടെടുക്കുന്നത് സാവധാനത്തിലാവുക (ഫോട്ടോസ്ട്രെസ് ടെസ്റ്റ്)
- വിഷ്വൽ അക്വിറ്റി ഗണ്യമായി കുറയുന്നു (രണ്ട് ലെവലോ അതിൽ കൂടുതലോ)
- മങ്ങിയ കാഴ്ച: നോൺ എക്സുഡേറ്റീവ് മാക്യുലർ ഡീജനറേഷൻ ഉള്ളവർ ലക്ഷണമില്ലാത്തവരാകാം അല്ലെങ്കിൽ അവരിൽ കാഴ്ച കുറയുന്നത് വളരെ പതുക്കെയാവാം, അതേസമയം എക്സുഡേറ്റീവ് മാക്കുലാർ ഡീജനറേഷൻ ഉള്ളവർ ദ്രുതഗതിയിലുള്ള കാഴ്ച നഷ്ടം (രക്തക്കുഴലുകളുടെ ചോർച്ചയും രക്തസ്രാവവും മറ്റും മൂലം) പലപ്പോഴും ശ്രദ്ധിക്കുന്നു.
- നിറങ്ങൾ വേർതിരിച്ചറിയാനുള്ള കഴിവ് കുറയുക, പ്രത്യേകിച്ച് ഇരുണ്ട നിറങ്ങൾ തമ്മിൽ അല്ലെങ്കിൽ, പല ഇളം നിറങ്ങൾ തമ്മിൽ.
- കോൺട്രാസ്റ്റ് സെൻസിറ്റിവിറ്റി നഷ്ടം.
- വിഷ്വൽ ഭ്രമാത്മകതകളും മിന്നുന്ന ഫ്ലാഷ് ലൈറ്റുകളും വെറ്റ് എഎംഡിയുടെ കടുത്ത കാഴ്ച നഷ്ടവുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു
മാക്യുലർ ഡീജനറേഷൻ പൂർണ്ണമായ അന്ധതയിലേക്ക് നയിക്കില്ല. ശരിക്കും പറഞ്ഞാൽ കാഴ്ച വൈകല്യമുള്ള വളരെ കുറച്ച് ആളുകൾ മാത്രമാണ് പൂർണ്ണമായും അന്ധർ. മിക്കവാറും എല്ലാവരിലും എല്ലാ സാഹചര്യങ്ങളിലും, ചില കാഴ്ച (പ്രധാനമായും പെരിഫറൽ കാഴ്ച) അവശേഷിക്കുന്നുണ്ടാവാം. ഗ്ലോക്കോമ പോലെയുള്ള സങ്കീർണ്ണമായ മറ്റ് അവസ്ഥകൾ പൂർണ്ണമായ അന്ധതയ്ക്ക് കാരണമാവാം, എന്നാൽ മാക്യുലർ ഡീജനറേഷൻ രോഗികൾക്ക് പൂർണ്ണമായി കാഴ്ചശക്തി നഷ്ടപ്പെടുന്നത് അപൂർവ്വമാണ്.[8]
മാക്കുലയുടെ വിസ്തീർണ്ണം റെറ്റിനയുടെ ആകെ വിസ്തീർണ്ണത്തിൻറെ 2.1% മാത്രമേയുള്ളൂ, ശേഷിക്കുന്ന 97.9% (പെരിഫറൽ ഫീൽഡ്) ഈ രോഗത്തെ ബാധിക്കുന്നില്ല. വിഷ്വൽ ഫീൽഡിന്റെ വളരെ ചെറിയ ഭാഗം മാത്രമാണ് മാക്യുലയ്ക്കുള്ളത് എങ്കിലും, വിഷ്വൽ കോർട്ടെക്സിന്റെ പകുതിയോളം ഭാഗം മാക്യുലർ വിവരങ്ങൾ പ്രോസസ്സ് ചെയ്യുന്നതിനായി നീക്കിവച്ചിരിക്കുന്നു.[9]
കേന്ദ്ര കാഴ്ച നഷ്ടപ്പെടുന്നത് വിഷ്വൽ പ്രവർത്തനത്തെ സാരമായി തന്നെ ബാധിക്കുന്നു. കേന്ദ്ര കാഴ്ചയില്ലാതെ പുസ്തകങ്ങളും മറ്റും വായിക്കുന്നത് തികച്ചും ബുദ്ധിമുട്ടാണ്. മാക്യുലർ ഡീജനറേഷന്റെ കേന്ദ്ര കാഴ്ച നഷ്ടത്തെ ഒരു കറുത്ത പുള്ളി ഉപയോഗിച്ച് കാണിക്കാൻ ശ്രമിക്കുന്ന ചിത്രങ്ങൾ (മുകളിൽ കോടുത്തര് പോലെ) യഥാർഥത്തിൽ ശരിക്കുള്ള വിഷ്വൽ നഷ്ടത്തിന്റെ വിനാശകരമായ സ്വഭാവത്തോട് നീതി പുലർത്തുന്നില്ല. ഒരു കടലാസിൽ അച്ചടിച്ച ആറ് ഇഞ്ച് ഉയരമുള്ള അക്ഷരങ്ങൾ, കണ്ണി നേരെ മുന്നിൽ പേപ്പർ ചരിച്ച് പിടിച്ച് വായിക്കാൻ ശ്രമിക്കുന്നതിലൂടെ ഇത് ഏകദേശം മനസ്സിക്കാം. മിക്ക ആളുകൾക്കും ഇത് ചെയ്യാൻ ബുദ്ധിമുട്ടാണ്.
കൂടാതെ, ഡ്രൈ മാക്യുലർ ഡീജനറേഷൻ ഉള്ള ആളുകൾക്ക് പലപ്പോഴും രോഗലക്ഷണങ്ങൾ അനുഭവപ്പെടില്ല, പക്ഷേ ഒന്നോ രണ്ടോ കണ്ണുകളിൽ മങ്ങിയ കാഴ്ചയുടെ ക്രമേണയുള്ള തുടക്കം അനുഭവപ്പെടാം.[10] [11] വെറ്റ് മാക്യുലർ ഡീജനറേഷൻ ഉള്ള ആളുകൾക്ക് തീവ്രമായ വിഷ്വൽ ലക്ഷണങ്ങൾ അനുഭവപ്പെടാം.
അപകടസാധ്യത ഘടകങ്ങൾ[തിരുത്തുക]
- വാർദ്ധക്യം : കൂടിയ പ്രായം എഎംഡിയുടെ ഏറ്റവും ശക്തമായ കാരണമാണ്, പ്രത്യേകിച്ച് 50 വയസ്സിനു മുകളിൽ.[12]
- കുടുംബ ചരിത്രം:
പരിസ്ഥിതിയും ജീവിതശൈലിയും[തിരുത്തുക]
- പുകവലി: പുകവലിയുള്ള ഒരാൾക്ക് മാക്യുലർ ഡീജനറേഷൻ വരാനുള്ള സാധ്യത പുകവക്കാത്ത ആളെക്കാൾ രണ്ട് മുതൽ മൂന്ന് മടങ്ങ് വരെ കൂടുതലാണ്. മാത്രമല്ല എഎംഡി ഒഴിവാക്കാനുള്ള കാര്യങ്ങളിൽ ഏറ്റവും പ്രഥാനം പുകവലിയാണ്. പുകവലിയും എഎംഡിയും തമ്മിലുള്ള ശക്തമായ ബന്ധം കണ്ടെത്തുന്ന പഠനങ്ങളുണ്ട്. സിഗരറ്റ് വലിക്കുന്നത് റെറ്റിനയിൽ വിഷാംശം ഉണ്ടാക്കാൻ സാധ്യതയുണ്ട്.[13]
- രക്താതിമർദ്ദം (ഉയർന്ന രക്തസമ്മർദ്ദം): 2013 ഏലിയനർ പഠനത്തിൽ, ആദ്യകാല അല്ലെങ്കിൽ വൈകി വരുന്ന എഎംഡിയും സിസ്റ്റോളിക് അല്ലെങ്കിൽ ഡയസ്റ്റോളിക് രക്തസമ്മർദ്ദം (ബിപി), രക്താതിമർദ്ദം അല്ലെങ്കിൽ ആന്റിഹൈപ്പർടെൻസിവ് മരുന്നുകളുടെ ഉപയോഗം എന്നിവയുമായി കാര്യമായി ബന്ധപ്പെടുന്നുണ്ട് എന്ന് കണ്ടെത്തിയിട്ടില്ല, എന്നാൽ ഉയർന്ന പൾസ് മർദ്ദം എഎംഡിയുടെ അപകടസാധ്യതയുമായി ഗണ്യമായി ബന്ധപ്പെട്ടിരിക്കുന്നു എന്ന് കരുതാം.[14]
- ആർത്തെറോസ്ലീറോസിസ് [15]
- ഉയർന്ന കൊളസ്ട്രോൾ: ഉയർന്ന കൊളസ്ട്രോൾ എഎംഡിയുടെ സാധ്യത വർദ്ധിപ്പിക്കും.[16]
- അമിതവണ്ണം: അമിതവണ്ണം ഒരു അപകട ഘടകമാണ്, പ്രത്യേകിച്ച് പുരുഷന്മാർക്കിടയിൽ.[17]
- കൊഴുപ്പ് കഴിക്കുന്നത്: പൂരിത കൊഴുപ്പുകൾ, ട്രാൻസ് ഫാറ്റ്, ഒമേഗ -6 ഫാറ്റി ആസിഡുകൾ എന്നിവയുൾപ്പെടെ ഉയർന്ന അളവിൽ ചില കൊഴുപ്പുകൾ കഴിക്കുന്നത് എഎംഡിക്ക് കാരണമാകാം, അതേസമയം മോണോസാച്ചുറേറ്റഡ് കൊഴുപ്പുകൾ സംരക്ഷിക്കാൻ സാധ്യതയുണ്ട്.[18] പ്രത്യേകിച്ച്, ഒമേഗ -3 ഫാറ്റി ആസിഡുകൾ എഎംഡിയുടെ സാധ്യത കുറയ്ക്കും.[19]
- സൂര്യപ്രകാശത്തിൽ നിന്നുള്ള അൾട്രാവയലറ്റ് ലൈറ്റ് എക്സ്പോഷർ എഎംഡി വരാനുള്ള സാധ്യതയുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു, തെളിവുകൾ മറ്റ് കാരണങ്ങളെ അപേക്ഷിച്ച് പക്ഷെ ദുർബലമാണ്.[11] [20]
- ഡിജിറ്റൽ സ്ക്രീൻ മനുഷ്യന്റെ കണ്ണുകൾക്ക് ദോഷകരമായ ഊർജ്ജം പുറപ്പെടുവിക്കുന്നില്ല, പക്ഷേ സ്ക്രീനിൽ ദീർഘനേരം നോക്കുന്നത് കണ്ണിന്റെ ബുദ്ധിമുട്ട് വർദ്ധിപ്പിക്കും. ഡിജിറ്റൽ സ്ക്രീൻ എക്സ്പോഷർ മാക്യുലർ ഡീജനറേഷന്റെ അപകടസാധ്യതയ്ക്ക് കാരണമാകുമെന്ന വാദത്തെ പിന്തുണയ്ക്കുന്നതിന് തെളിവുകളൊന്നുമില്ല.[21]
ജനിതകശാസ്ത്രം[തിരുത്തുക]
ബാധിത വ്യക്തിയുടെ സഹോദരങ്ങൾക്കുള്ള ആവർത്തന അനുപാതം സാധാരണ ജനസംഖ്യയേക്കാൾ മൂന്ന് മുതൽ ആറ് മടങ്ങ് വരെ കൂടുതലാണ്. [22] ജനിതക ലിങ്കേജ് വിശകലനത്തിലൂടെ വ്യത്യസ്ത ക്രോമസോമുകളിൽ (1, 6, 10) മൂന്ന് സ്ഥലങ്ങളിൽ 5 സെറ്റ് ജീൻ വകഭേദങ്ങൾ കണ്ടെത്തി, ഇത് കുറഞ്ഞത് 50% അപകടസാധ്യത വിശദീകരിക്കുന്നു. ഈ ജീനുകൾക്ക് രോഗപ്രതിരോധ പ്രതികരണം, കോശജ്വലന പ്രക്രിയകൾ, റെറ്റിനയുടെ ഹോമിയോസ്റ്റാസിസ് എന്നിവ നിയന്ത്രിക്കുന്ന റോളുകളുണ്ട്. ഈ ജീനുകളുടെ വകഭേദങ്ങൾ ഈ പ്രക്രിയകളിൽ പലതരം അപര്യാപ്തതകൾക്ക് കാരണമാകുന്നു. കാലക്രമേണ, ഇത് മൂലം ഇൻട്രാ സെല്ലുലാർ, എക്സ്ട്രാ സെല്ലുലാർ മെറ്റബോളിക് അവശിഷ്ടങ്ങൾ അടിഞ്ഞു കൂടുന്നു. ഇത് റെറ്റിനയിൽ പാടുകൾ ഉണ്ടാക്കുകയോ വാസ്കുലറൈസേഷന്റെ തകർച്ചയ്ക്ക് കാരണമാകുകയോ ചെയ്യും.
ഈ ജീൻ വ്യതിയാനങ്ങളിൽ ചിലത് തിരിച്ചറിയാൻ ജനിതക പരിശോധനകൾ ലഭ്യമാണ്. എന്നിരുന്നാലും, ജനിതകശാസ്ത്രം, പരിസ്ഥിതി, ജീവിതശൈലി എന്നിവ തമ്മിലുള്ള സങ്കീർണ്ണമായ ഇടപെടലാണ് മാക്യുലർ ഡീജനറേഷന്റെ രോഗകാരി, അതിനാൽ തന്നെ അനുകൂലമല്ലാത്ത ജനിതക ഘടകങ്ങളുടെ സാന്നിധ്യം കൊണ്ട് മാത്രം രോഗത്തിൻറെ പുരോഗതി പ്രവചിക്കാൻ സാധ്യമല്ല. തിരിച്ചറിഞ്ഞ ജീൻ വകഭേദങ്ങൾ കണ്ടെത്തിയ മൂന്ന് ലോക്കികൾ ഇനിപ്പറയുന്നവയാണ്::
- 1q31.3 സ്ഥാനത്ത് ക്രോമസോം 1 ലെ കോംപ്ലിമെന്റ് ഫാക്ടർ എച്ച് (സിഎഫ്എച്ച്)[23]
- 10q26 സ്ഥാനത്ത് ക്രോമസോം 10 ലെ എച്ച്ടിആർഎ സെറീൻ പെപ്റ്റിഡേസ് 1 / പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലോപ്പതി സസ്പെസിബിലിറ്റി 2 (HTRA1 / ARMS2)
- 6p21.3 സ്ഥാനത്ത് ക്രോമസോം 6 ലെ കോംപ്ലിമെന്റ് ഫാക്ടർ ബി / കോംപ്ലിമെന്റ് കോമ്പോണന്റ് 2 (സിഎഫ്ബി / സിസി 2)
നിർദ്ദിഷ്ട ജീനുകൾ[തിരുത്തുക]
- കോംപ്ലിമെന്റ് സിസ്റ്റം പ്രോട്ടീനുകൾക്കുള്ള ജീനുകളിലെ പോളിമോർഫിസങ്ങൾ: കോംപ്ലിമെന്റ് സിസ്റ്റം പ്രോട്ടീൻ ഫാക്ടർ എച്ച് (സിഎഫ്എച്ച്), ഫാക്ടർ ബി (സിഎഫ്ബി), ഫാക്ടർ 3 (സി 3) എന്നിവയ്ക്കുള്ള ജീനുകൾ എഎംഡി വരാനുള്ള ഒരു വ്യക്തിയുടെ അപകടസാധ്യതയുമായി ശക്തമായി ബന്ധപ്പെട്ടിരിക്കുന്നു. കോശജ്വലന പ്രതികരണത്തെ തടയുന്നതിൽ CFH ഉൾപ്പെടുന്നു. CFH ( Y402H ) ലെ മ്യൂട്ടേഷൻ, റെറ്റിന പോലുള്ള നിർണായക പ്രതലങ്ങളിൽ പൂരകത്തെ നിയന്ത്രിക്കാനുള്ള CFH ന്റെ കഴിവ് കുറയ്ക്കുകയും മാക്കുലയ്ക്കുള്ളിൽ കോശജ്വലന പ്രതികരണത്തിലേക്ക് നയിക്കുകയും ചെയ്യുന്നു. കോമ്പ്ലിമെൻറ് ഫാക്റ്റർ എച്ച് അനുബന്ധ ജീനുകളായ ആർ 3, ആർ 1 എന്നിവയുടെ അഭാവം എഎംഡിയിൽ നിന്നും സംരക്ഷിക്കുന്നു.[24] [25] 2007 ലെ രണ്ട് സ്വതന്ത്ര പഠനങ്ങളിൽ സി 3 ജീനിലെ ഒരു സാധാരണ മ്യൂട്ടേഷൻ Arg80Gly, മാക്യുലർ ഡീജനറേഷനുമായി ശക്തമായി ബന്ധപ്പെട്ടിരിക്കുന്നു എന്ന് കണ്ടെത്തി.[26] [27] ഈ രോഗത്തിന്റെ രോഗകാരിയിൽ പൂരക പാതയുടെ സ്വാധീനം അടിവരയിടുന്നതിനായി രണ്ട് പേപ്പറുകളുടെയും രചയിതാക്കൾ സൂചിപ്പിക്കുന്നു.
- 2006 ലെ രണ്ട് പഠനങ്ങളിൽ, എച്ച്ടിആർഎ 1 (എൻകോഡിംഗ് എ സെക്രീൻ സെറീൻ പ്രോട്ടീസ്) എന്ന രോഗത്തെ ബാധിക്കുന്ന മറ്റൊരു ജീൻ തിരിച്ചറിഞ്ഞു.[28] [29]
- SERPING1 (സെർപിൻ പെപ്റ്റിഡേസ് ഇൻഹിബിറ്റർ, ക്ലേഡ് ജി (സി 1 ഇൻഹിബിറ്റർ), അംഗം 1) എന്ന ജീനിന്റെ ആറ് മ്യൂട്ടേഷനുകൾ മാക്യുലർ ഡീജനറേഷനുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു. ഈ ജീനിലെ മ്യൂട്ടേഷനുകൾ പാരമ്പര്യ ആൻജിയോഡീമയ്ക്കും കാരണമാകും.
- ഫൈബുലിൻ -5 മ്യൂട്ടേഷൻ: ഫിബുലിൻ -5 ലെ ജനിതക വൈകല്യങ്ങൾ മൂലം രോഗത്തിന്റെ അപൂർവ രൂപങ്ങൾ ഓട്ടോസോമൽ ഡോമിനൻറ് രീതിയിൽ വരുന്നുണ്ട്. 2004 ൽ സ്റ്റോൺ തുടങ്ങിയവർ 402 എഎംഡി രോഗികളിൽ ഒരു സ്ക്രീൻ നടത്തുകയും ഫിബുലിൻ -5 ലെ മ്യൂട്ടേഷനുകളും രോഗവും തമ്മിലുള്ള ബന്ധത്തിൻറെ പ്രാധാന്യം വെളിപ്പെടുത്തി.
മൈറ്റോകോൺഡ്രിയലുമായി ബന്ധപ്പെട്ട ജീൻ പോളിമോർഫിസങ്ങൾ[തിരുത്തുക]
മേൽ പറഞ്ഞത് MT-ND2 തന്മാത്രയിൽ ഉണ്ടെങ്കിൽ വെറ്റ് എഎംഡിക്ക് സാധ്യതയുണ്ട്.[30]
പാത്തോഫിസിയോളജി[തിരുത്തുക]
ഓക്സിഡേറ്റീവ് സ്ട്രെസ്, മൈറ്റോകോണ്ട്രിയൽ ഡിസ്ഫംഗ്ഷൻ, കോശജ്വലന പ്രക്രിയകൾ എന്നിവയുൾപ്പെടെ ചില സിദ്ധാന്തങ്ങൾ മുന്നോട്ട് വച്ചിട്ടുണ്ടെങ്കിലും പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷന്റെ രോഗകാരിയെക്കുറിച്ച് കൂടുതൽ അറിവില്ല.
കേടായ സെല്ലുലാർ ഘടകങ്ങളുടെ ഉൽപാദനവും അധപതനവും തമ്മിലുള്ള അസന്തുലിതാവസ്ഥ, ഇൻട്രാ സെല്ലുലാർ ലിപ്പോഫുസ്സിൻ, എക്സ്ട്രാ സെല്ലുലാർ ഡ്രുസെൻ പോലെയുള്ള ദോഷകരമായ ഉൽപ്പന്നങ്ങളുടെ ശേഖരണത്തിലേക്ക് നയിക്കുന്നു. എഎംഡിയുടെ പ്രാരംഭ ഘട്ടത്തിൽ ജോഗ്രഫിക്കൽ അട്രോഫിക്ക് മുമ്പുള്ള റെറ്റിനൽ പിഗ്മെൻറ് എപ്പിത്തീലിയം (ആർപിഇ) കനം കുറയൽ അല്ലെങ്കിൽ ഡിപിഗ്മെൻറേഷൻ മേഖലകളാണ് ഇൻസിപിയന്റ് അട്രോഫി എന്ന് വിളിക്കുന്നത്. എഎംഡിയുടെ വിപുലമായ ഘട്ടങ്ങളിൽ, ആർപിഇയുടെ അട്രോഫി (ജിയോഗ്രാഫിക് അട്രോഫി) കൂടാതെ / അല്ലെങ്കിൽ പുതിയ രക്തക്കുഴലുകളുടെ വളർച്ച (നിയോവാസ്കുലറൈസേഷൻ) എന്നിവയുടെ ഫലമായി ഫോട്ടോറിസെപ്റ്ററുകളുടെ മരണത്തിനും കേന്ദ്ര കാഴ്ച നഷ്ടത്തിനും കാരണമാകുന്നു.
ഡ്രൈ (നോൺ എക്സുഡേറ്റീവ്) രൂപത്തിൽ, ഡ്രൂസെൻ എന്നറിയപ്പെടുന്ന സെല്ലുലാർ അവശിഷ്ടങ്ങൾ റെറ്റിനയ്ക്കും കോറോയിഡിനുമിടയിൽ അടിഞ്ഞു കൂടുന്നു, ഇത് റെറ്റിനയിൽ അട്രോഫിയും പാടുകളും ഉണ്ടാക്കുന്നു. കൂടുതൽ കഠിനമായ വെറ്റ് (എക്സുഡേറ്റീവ്) രൂപത്തിൽ, റെറ്റിനയുടെ പിന്നിലുള്ള കോറോയിഡിൽ നിന്ന് രക്തക്കുഴലുകൾ വളരുന്നു (നിയോവാസ്കുലറൈസേഷൻ) , ഇത് എക്സുഡേറ്റും ദ്രാവകവും ചോർന്ന് രക്തസ്രാവത്തിനും കാരണമാകുന്നു.
ഇമ്മ്യൂൺ മീഡിയേറ്ററുകളുടെ ഒരു കൂട്ടം ഡ്രൂസനിൽ ധാരാളം ഉണ്ടെന്ന് ആദ്യകാല പ്രവർത്തനങ്ങൾ തെളിയിച്ചിട്ടുണ്ട്.[31] കോംപ്ലിമെന്റ് ഫാക്ടർ എച്ച് (സിഎഫ്എച്ച്) ഈ കോശജ്വലന കാസ്കേഡിന്റെ ഒരു പ്രധാന തടസ്സമാണ്, കൂടാതെ സിഎഫ്എച്ച് ജീനിലെ രോഗവുമായി ബന്ധപ്പെട്ട പോളിമോർഫിസം എഎംഡിയുമായി ശക്തമായി ബന്ധപ്പെട്ടിരിക്കുന്നു.[32] [33] [34] [35] [36] അങ്ങനെ ക്രോണിക് ലോ ഗ്രേഡ് കോംപ്ലിമെന്റ് ആക്റ്റിവേഷന്റെയും മാക്യുലയിലെ വീക്കത്തിന്റെയും എഎംഡി പാത്തോഫിസിയോളജിക്കൽ മോഡൽ വികസിപ്പിച്ചെടുത്തു.[37] [38] കോംപ്ലിമെന്റ് ഘടകം 3 (സി 3) ഉൾപ്പെടെയുള്ള കോംപ്ലിമെന്റ് കാസ്കേഡിന്റെ മറ്റ് ഘടകങ്ങളിൽ രോഗവുമായി ബന്ധപ്പെട്ട ജനിതക പോളിമോർഫിസങ്ങൾ കണ്ടെത്തിയതാണ് ഇതിന് വിശ്വാസ്യത നൽകുന്നത്.[39]
എഎംഡിയുടെ ശക്തമായ പ്രവചനം എൽഒസി 387715 ൽ ക്രോമസോം 10q26 ൽ കണ്ടെത്തി. ഈ സൈറ്റിലെ ഉൾപ്പെടുത്തൽ / ഇല്ലാതാക്കൽ പോളിമോർഫിസം ARMS2 ജീനിന്റെ ആവിഷ്കാരത്തെ കുറയ്ക്കുന്നു, പക്ഷേ പോളിഅഡൈനിലേഷൻ സിഗ്നൽ ഇല്ലാതാക്കുന്നതിലൂടെ അതിന്റെ എംആർഎൻഎയെ അസ്ഥിരപ്പെടുത്തുന്നു.[40] ARMS2 പ്രോട്ടീൻ മൈറ്റോകോൺഡ്രിയയിലേക്ക് പ്രാദേശികവൽക്കരിക്കപ്പെടുകയും ഊർജ്ജ രാസവിനിമയത്തിൽ പങ്കാളികളാകുകയും ചെയ്യാം, എന്നിരുന്നാലും അതിന്റെ പ്രവർത്തനത്തെക്കുറിച്ച് ഇനിയും വളരെയധികം കണ്ടെത്താനുണ്ട്.
എഎംഡി പുരോഗതിയിൽ എക്സ്ട്രാ സെല്ലുലാർ മാട്രിക്സ് മെറ്റബോളിസത്തിന് ഒരു പങ്ക് നിർദ്ദേശിക്കുന്ന മെറ്റലോപ്രോട്ടിനേസ് 3 ( ടിഎംപി 3) ന്റെ ടിഷ്യു ഇൻഹിബിറ്റർ പുരോഗതി അപകടസാധ്യതയുടെ മറ്റ് ജീൻ മാർക്കറുകളിൽ ഉൾപ്പെടുന്നു.[41] കൊളസ്ട്രോൾ മെറ്റബോളിസിംഗ് ജീനുകളായ ഹെപ്പാറ്റിക് ലിപേസ്, കൊളസ്ട്രോൾ ഈസ്റ്റർ ട്രാൻസ്ഫേറസ്, ലിപ്പോപ്രോട്ടീൻ ലിപേസ്, എടിപി-ബൈൻഡിംഗ് കാസറ്റ് എ 1 എന്നിവ രോഗത്തിന്റെ പുരോഗതിയുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു. രോഗത്തിന്റെ ആദ്യകാല ലക്ഷണമായ ഡ്രൂസെൻ കൊളസ്ട്രോൾ കൊണ്ട് സമ്പന്നമാണ്, ഇത് ജീനോം-വൈഡ് അസോസിയേഷൻ പഠനങ്ങളുടെ ഫലങ്ങൾക്ക് സാധുത നൽകുന്നു.[42]
ഘട്ടങ്ങൾ[തിരുത്തുക]
എഎംഡിയിൽ റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിനും അന്തർലീനമായ കോറോയിഡിനുമിടയിൽ, മാക്യുലയിൽ (റെറ്റിനയുടെ ഒരു ഭാഗം) ഡ്രൂസെൻ (എക്സ്ട്രാ സെല്ലുലാർ പ്രോട്ടീനുകളുടെയും ലിപിഡുകളുടെയും നിർമ്മാണം) എന്ന സ്വഭാവ സവിശേഷതകളുള്ള മഞ്ഞ നിക്ഷേപങ്ങൾ പുരോഗമിക്കുന്നു. ഈ ശേഖരണം കാലക്രമേണ റെറ്റിനയെ തകരാറിലാക്കുമെന്ന് വിശ്വസിക്കപ്പെടുന്നു. എഎംഡിയിൽ അടിഞ്ഞുകൂടുന്ന പ്രോട്ടീനുകളിലൊന്നാണ് അൽഷിമേഴ്സ് രോഗത്തിൽ തലച്ചോറിൽ വളരുന്ന അമിലോയിഡ് ബീറ്റ, ഇത് കാരണം എഎംഡിയെ ചിലപ്പോൾ "കണ്ണിന്റെ അൽഷിമേഴ്സ്" അല്ലെങ്കിൽ "റെറ്റിനയുടെ അൽഷിമേഴ്സ്" എന്ന് വിളിക്കുന്നു.[43] ഡ്രൂസന്റെ വ്യാപ്തിയെ (വലുപ്പവും എണ്ണവും) ഭാഗികമായി അടിസ്ഥാനമാക്കി എഎംഡിയെ, ഏർളി, ഇന്റർമീഡിയറ്റ്, ലേറ്റ് എന്നിങ്ങനെ 3 ഘട്ടങ്ങളായി തിരിക്കാം. [1]
റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിനും അന്തർലീനമായ കോറോയിഡിനുമിടയിൽ മാക്യുലയിലെെ ചെറിയ മഞ്ഞ നിക്ഷേപങ്ങളിൽ (ഡ്രൂസെൻ) എഎംഡി പത്തോളജി ആരംഭിക്കുന്നു. ഈ ആദ്യകാല മാറ്റങ്ങളുള്ള മിക്ക ആളുകൾക്കും നല്ല കാഴ്ചയുണ്ടാവും. ഡ്രൂസെൻ ഉള്ള ആളുകൾക്ക് മാക്യുലർ ഡീജനറേഷൻ ഉണ്ടാവാനും ഉണ്ടാവാതിരിക്കാനും സാധ്യതയുണ്ട്. വാസ്തവത്തിൽ, 60 വയസ്സിനു മുകളിലുള്ള ഭൂരിഭാഗം ആളുകളും പ്രതികൂല ഫലങ്ങളില്ലാതെ മദ്യപിക്കുന്നു. ഡ്രൂസൻ വലുതും കൂടുതലും ആണെങ്കിൽ ലക്ഷണങ്ങൾ ഉണ്ടാകാനുള്ള സാധ്യത കൂടുതലാണ്, ഇത് മാക്കുലയ്ക്ക് കീഴിലുള്ള പിഗ്മെന്റ് സെൽ പാളിയിലെ അസ്വസ്ഥതയുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു. വലുതും മൃദുവായതുമായ ഡ്രൂസൻ ഉയർന്ന കൊളസ്ട്രോൾ നിക്ഷേപവുമായി ബന്ധപ്പെട്ടതാണെന്ന് കരുതപ്പെടുന്നു.
ഏർളി എഎംഡി[തിരുത്തുക]
ഒരു ശരാശരി മനുഷ്യ മുടിയുടെ വീതിയോളമുള്ള ഇടത്തരം വലിപ്പമുള്ള ഡ്രൂസന്റെ സാന്നിധ്യം അടിസ്ഥാനമാക്കിയാണ് ആദ്യകാല എഎംഡി നിർണ്ണയിക്കുന്നത്. ആദ്യകാല എഎംഡിക്ക് സാധാരണയായി ലക്ഷണങ്ങളില്ല.[1]
ഇന്റർമീഡിയറ്റ് എഎംഡി[തിരുത്തുക]
വലിയ ഡ്രൂസൻ കൂടാതെ/അല്ലെങ്കിൽ ഏതെങ്കിലും റെറ്റിന പിഗ്മെന്റ് അസാധാരണതകൾ ഇവ ഒരുമിച്ചു വന്നാലാണ് ഇന്റർമീഡിയറ്റ് എഎംഡി എന്ന് പറയുന്നത്. ഇന്റർമീഡിയറ്റ് എഎംഡി മൂഒലം കുറച്ച് കാഴ്ച നഷ്ടപ്പെടാൻ കാരണമായേക്കാം, എന്നാലും ആദ്യകാല എഎംഡി പോലെ, ഇത് സാധാരണയായി അധികം ലക്ഷണങ്ങളില്ലാത്തതാണ്.[1] [44]
ലേറ്റ് എ.എം.ഡി.[തിരുത്തുക]
എഎംഡിയുടെ അവസാനത്തിൽ, മതിയായ റെറ്റിന കേടുപാടുകൾ സംഭവിക്കുന്നു, ഡ്രൂസന് പുറമേ, ആളുകൾക്ക് രോഗലക്ഷണമായ കേന്ദ്ര കാഴ്ച നഷ്ടം അനുഭവപ്പെടാൻ തുടങ്ങും. കാഴ്ച നഷ്ടത്തിന് കാരണം ഒന്നുകിൽ അട്രോഫിയുടെ വികസനം അല്ലെങ്കിൽ നിയോവാസ്കുലർ രോഗത്തിന്റെ ആരംഭം എന്നിവ ആകാം. നാശനഷ്ടങ്ങളെ അടിസ്ഥാനമാക്കി എഎംഡിയെ രണ്ട് ഉപവിഭാഗങ്ങളായി തിരിച്ചിരിക്കുന്നു: ജിയോഗ്രാഫിക് അട്രോഫി, വെറ്റ് എഎംഡി (നിയോവാസ്കുലർ എഎംഡി എന്നും ഇതിനെ വിളിക്കുന്നു). [44] [1]
ഡ്രൈ എഎംഡി[തിരുത്തുക]
നിയോവാസ്കുലർ (വെറ്റ് എഎംഡി) അല്ലാത്ത എല്ലാത്തരം എഎംഡികളെയും ഉൾക്കൊള്ളുന്ന വിശാലമായ പദവിയാണ് ഡ്രൈ എഎംഡി (നോൺഎക്സുഡേറ്റീവ് എഎംഡി എന്നും അറിയപ്പെടുന്നു). എഎംഡിയുടെ ആദ്യകാല, ഇന്റർമീഡിയറ്റ് രൂപങ്ങളും ജിയോഗ്രാഫിക് അട്രോഫി എന്നറിയപ്പെടുന്ന വരണ്ട എഎംഡിയുടെ വിപുലമായ രൂപവും ഇതിൽ ഉൾപ്പെടുന്നു. ഡ്രൈ എഎംഡി രോഗികൾക്ക് ആദ്യഘട്ടത്തിൽ കുറഞ്ഞ ലക്ഷണങ്ങളുണ്ടാകും; ഈ അവസ്ഥ ജോഗ്രഫിക്കൽ അട്രോഫിയിലേക്ക് മുന്നേറുകയാണെങ്കിൽ വിഷ്വൽ ഫംഗ്ഷൻ നഷ്ടം പലപ്പോഴും സംഭവിക്കാറുണ്ട്. ഡ്രൈ എഎംഡി 80-90% കേസുകൾക്ക് കാരണമാവുകയും സാവധാനത്തിൽ പുരോഗമിക്കുകയും ചെയ്യുന്നു. 10-20% ആളുകളിൽ, വരണ്ട എഎംഡി നനഞ്ഞ തരത്തിലേക്ക് പുരോഗമിക്കുന്നു.
ജിയോഗ്രഫിക്ക് അട്രോഫി[തിരുത്തുക]
ജിയോഗ്രാഫിക് അട്രോഫി (എട്രോഫിക് എഎംഡി എന്നും അറിയപ്പെടുന്നു) എഎംഡിയുടെ ഒരു നൂതന രൂപമാണ്, അതിൽ റെറ്റിന കോശങ്ങളുടെ സ്ഥായിയായ നഷ്ടം വിഷ്വൽ ഫംഗ്ഷൻ നഷ്ടപ്പെടുന്നതിലേക്ക് നയിക്കുന്നു. റെറ്റിനയെ നിർമ്മിക്കുന്ന ഒന്നിലധികം പാളികളുണ്ട്, ജിയോഗ്രഫിക്ക് അട്രോഫിയിൽ, അട്രോഫിക്ക് വിധേയമാകുന്ന മൂന്ന് നിർദ്ദിഷ്ട പാളികളുണ്ട്: കൊറിയോകാപിലറിസ്, റെറ്റിനൽ പിഗ്മെൻറ് എപ്പിത്തീലിയംം, ഫോട്ടോറിസെപ്റ്ററുകൾ എന്നിവയാണ് അത്.
ജിയോഗ്രഫിക്ക് അട്രോഫിയിൽ അട്രോഫിക്ക് വിധേയമാകുന്ന മൂന്ന് പാളികൾ എല്ലാം പരസ്പരം ചേർന്നാണ്. ഫോട്ടോറിസെപ്റ്ററുകൾ ഏറ്റവും പുറമേയുള്ളതാണ്, അവ പുറം ലോകത്തിൽ നിന്നുള്ള പ്രകാശത്തിൽ നിന്ന് ഊർജ്ജത്തെ തലച്ചോറിലേക്ക് അയയ്ക്കുന്നതിനുള്ള ഒരു വൈദ്യുത സിഗ്നലാക്കി മാറ്റാൻ കാരണമാകുന്ന കോശങ്ങളാണ്. റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിന്റെ നിരവധി പ്രവർത്തനങ്ങൾ ഉണ്ട്. റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിന്റെ പ്രധാന പ്രവർത്തനങ്ങളിലൊന്ന് ഓക്സിഡേറ്റീവ് സ്ട്രെസ് കുറയ്ക്കുക എന്നതാണ്. പ്രകാശം ആഗിരണം ചെയ്തുകൊണ്ട് അത് അങ്ങനെ ചെയ്യുന്നു, അങ്ങനെ അത് അടിസ്ഥാന പാളികളിലേക്ക് എത്തുന്നത് തടയുന്നു. റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിന് കീഴിലുള്ള പാളികൾ വളരെ വാസ്കുലറൈസ് ചെയ്തതിനാൽ അവയ്ക്ക് ഉയർന്ന ഓക്സിജൻ ടെൻഷനുണ്ട്. അതിനാൽ, പ്രകാശം ആ പാളികളിലേക്ക് എത്തുകയാണെങ്കിൽ, നിരവധി ഫ്രീ റാഡിക്കലുകൾ രൂപപ്പെടുകയും സമീപത്തുള്ള ടിഷ്യൂകൾക്ക് നാശമുണ്ടാക്കുകയും ചെയ്യും. ജിയോഗ്രഫിക്ക് അട്രോഫിയിൽ അട്രോഫിക്ക് വിധേയമാകുന്ന ഏറ്റവും ആഴത്തിലുള്ള പാളിയെ കൊറിയോകാപ്പിലറിസ് എന്ന് വിളിക്കുന്നു. റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിന് പോഷകങ്ങൾ നൽകുന്ന ഒരു കാപ്പിലറി നെറ്റ്വർക്കാണ് ഇത്.
ജിയോഗ്രഫിക്ക് അട്രോഫിയുടെ പാത്തോഫിസിയോളജി ഇപ്പോഴും അനിശ്ചിതത്വത്തിലാണ്. റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയം കുറവായതിനാലാണോ ഓക്സിഡേറ്റീവ് സ്ട്രെസ് വർദ്ധിക്കുന്നതെന്ന് ചില പഠനങ്ങൾ ചോദ്യം ചെയ്യുന്നു.[45] മറ്റ് പഠനങ്ങൾ നാശനഷ്ടങ്ങളുടെ ഇൻഫ്ലമേറ്ററി കാരണങ്ങൾ ആണ് അന്വേഷിച്ചത്. [46] ഇതുവരെ, മെഡിക്കൽ സമൂഹം ഈ വിഷയത്തിൽ കൃത്യമായ തീർപ്പിലെത്തിയിട്ടില്ല. സമീപകാല പഠനങ്ങൾ ഓരോ ലെയറുകളെയും വ്യക്തിഗതമായി കാണാൻ തുടങ്ങി. കൊറിയോകാപിലറികളിലെ രക്തയോട്ടം കുറയുന്നത് റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിന്റെയും ഫോട്ടോറിസെപ്റ്ററുകളുടെയും അട്രോഫിക്ക് മുന്നേസംഭവിക്കുന്നുവെന്ന് കണ്ടെത്തിയിട്ടുണ്ട്.[47] കൊറിയോകാപിലറി ഒരു വാസ്കുലർ ലെയറായതിനാൽ, രക്തയോട്ടം കുറയുന്നതുമൂലം ജിയോഗ്രഫിക്ക് അട്രോഫി വരാനുള്ള കാരണമായി ഇത് കണക്കാക്കാം.
വെറ്റ് എഎംഡി[തിരുത്തുക]
നൂതന എഎംഡിയുടെ "വെറ്റ്" രൂപമായ നിയോവാസ്കുലർ അല്ലെങ്കിൽ എക്സുഡേറ്റീവ് എഎംഡിയിൽ, ബ്രച്സ് മെംബ്രേൻ വഴി കോറിയോകാപില്ലാരിസിലെ അസാധാരണമായ രക്തക്കുഴലുകളുടെ വളർച്ച (കോറോയ്ഡൽ നിയോവാസ്കുലറൈസേഷൻ) മൂലം കാഴ്ച നഷ്ടപ്പെടാൻ കാരണമാകുന്നു. ഇത് സാധാരണയായി എഎംഡിയുടെ ഡ്രൈ രൂപത്തിന് മുമ്പാണ് കാണുന്നത്, പക്ഷേ എല്ലായ്പ്പോഴും അങ്ങനെ ആവണമെന്നില്ല. റെറ്റിനയിലെ അസാധാരണമായ രക്തക്കുഴലുകളുടെ വ്യാപനം വാസ്കുലർ എൻഡോതെലിയൽ ഗ്രോത്ത് ഫാക്ടർ (വിഇജിഎഫ്) ഉത്തേജിപ്പിക്കുന്നു. ഈ രക്തക്കുഴലുകൾ അസാധാരണമായതിനാൽ ഇവ സാധാരണ രക്തക്കുഴലുകളേക്കാൾ ദുർബലമാണ്, ഇത് മാക്യുലയ്ക്ക് താഴെയുള്ള രക്തത്തിലേക്കും പ്രോട്ടീൻ ചോർച്ചയിലേക്കും നയിക്കുന്നു. ഈ രക്തക്കുഴലുകളിൽ നിന്നുള്ള രക്തസ്രാവം, ചോർച്ച, പാടുകൾ എന്നിവ ഒടുവിൽ ഫോട്ടോറിസെപ്റ്ററുകൾക്ക് മാറ്റാനാവാത്ത തകരാറുണ്ടാക്കുകയും ചികിത്സിച്ചില്ലെങ്കിൽ കാഴ്ചശക്തി കുറയുകയും ചെയ്യും.
ഓക്സിഡേറ്റീവ് സ്ട്രെസ്[തിരുത്തുക]
റെറ്റിനൽ പിഗ്മെന്റ് എപിത്തീലിയത്തിലെ (ആർപിഇ) ലൈസോസോമുകൾക്കുള്ളിലെ കുറഞ്ഞ തന്മാത്രാ-ഭാരം, ഫോട്ടോടോക്സിക്, പ്രോ-ഓക്സിഡൻറ് മെലാനിൻ ഒലിഗോമറുകൾ എന്നിവയുടെ പ്രായവുമായി ബന്ധപ്പെട്ട ശേഖരണം ആർപിഇ - ഓട്ടോഫാഗി വഴി ഫോട്ടോറെസെപ്റ്റർ ഔറ്റർ റോഡ് സെഗ്മെന്റുകളുടെ (പിഒഎസ്) ദഹനനിരക്ക് കുറയ്ക്കുന്നതിന് കാരണമാകാം. പിഒഎസിന്റെ ദഹനനിരക്കിന്റെ കുറവ് ലിപോഫുസ്സിൻ രൂപീകരണവുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു - ഇത് എഎംഡിയുമായി ബന്ധപ്പെട്ട ഒരു ക്ലാസിക് അടയാളമാണ്.[48]
പുകവലിക്കാരിലും അൾട്രാവയലറ്റ് വികിരണത്തിന് വിധേയരായവരിലും രോഗത്തിന്റെ വർദ്ധിച്ച നിരക്ക്, എഎംഡിയുടെ കാരണത്തിൽ റെറ്റിനൽ ഓക്സിഡേറ്റീവ് സ്ട്രെസിന്റെ പങ്ക് സൂചിപ്പിക്കുന്നു.[13] [49] [50]
മൈറ്റോകോൺഡ്രിയൽ ഡിസ്ഫങ്ഷനും ഇതിൽ ഒരു പങ്കുണ്ടാകാം.[51]
രോഗനിർണയം[തിരുത്തുക]

പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷൻ രോഗ നിർണ്ണയം കാഴ്ച പരിശോധനയേക്കാളുപരി മാക്യുലയിലെ ലക്ഷണങ്ങളുടെ പരിശോധനയാണ്. വെറ്റ് എഎംഡി സാധാരണയായി ഡ്രൈ എഎംഡിയുടെ വിപുലമായ പുരോഗതിയാണ്, അതിൻറെ പരിശോധനയ്ക്ക് അധിക ഡയഗ്നോസ്റ്റിക് ഉപകരണങ്ങൾ ആവശ്യമാണ്. വെറ്റ് എഎംഡിയുടെ ആദ്യകാല രോഗനിർണയം കാഴ്ചശക്തി വീണ്ടും കുറയാതിരിക്കാനും കാഴ്ച മെച്ചപ്പെടുത്തുന്നതിനും സഹായിക്കുന്നു.[52]
ഡ്രൈ (അല്ലെങ്കിൽ പ്രാരംഭ ഘട്ടത്തിൽ) എഎംഡി രോഗനിർണയത്തിൽ ഇനിപ്പറയുന്ന ക്ലിനിക്കൽ പരിശോധനകളും നടപടിക്രമങ്ങളും പരിശോധനകളും ഉൾപ്പെടാം:
- ഡ്രൈയിൽ നിന്നും വെറ്റ് എഎംഡിയിലേക്കുള്ള മാറ്റം അതിവേഗം സംഭവിക്കാം, ഇത് ചികിത്സിച്ചില്ലെങ്കിൽ ആറുമാസത്തിനുള്ളിൽ നിയമപരമായ അന്ധതയ്ക്ക് വരെ കാരണമാകും. ഇത് സംഭവിക്കുന്നത് തടയുന്നതിനും രോഗ പ്രക്രിയയിൽ നേരത്തെ പ്രതിരോധ തന്ത്രങ്ങൾ ആരംഭിക്കുന്നതിനും ഡാർക്ക് അഡാപ്റ്റേഷൻ പരിശോധന നടത്താം. ഡാർക്ക് അഡാപ്റ്റോമീറ്ററിന് സബ്ക്ലിനിക്കൽ എഎംഡി ചികിത്സാപരമായി പ്രകടമാകുന്നതിനേക്കാൾ കുറഞ്ഞത് മൂന്ന് വർഷം മുമ്പെങ്കിലും കണ്ടെത്താനാകും.[53]
- ദൃശ്യതീവ്രത സംവേദനക്ഷമത നഷ്ടപ്പെടുന്നതിനാൽ കോണ്ടറുകൾ, ഷാഡോകൾ, വർണ്ണ ദർശനം എന്നിവ കുറയും. കോൺട്രാസ്റ്റ് സെൻസിറ്റിവിറ്റിയിലെ നഷ്ടം പെല്ലി റോബ്സൺ പോലുള്ള കോൺട്രാസ്റ്റ് സെൻസിറ്റിവിറ്റി ടെസ്റ്റ് വീട്ടിലോ കണ്ണ് സ്പെഷ്യലിസ്റ്റിൻറെ അടുത്ത് നടത്തി വേഗത്തിലും എളുപ്പത്തിലും അളക്കാൻ കഴിയും.
- ഒരു ആംസ്ലർ ഗ്രിഡ് കാണുമ്പോൾ, ചില നേർരേഖകൾ അലകളായും, ചില പാച്ചുകൾ ശൂന്യമായും ദൃശ്യമാകും
- ഒരു സ്നെല്ലെൻ ചാർട്ട് കാഴ്ച പരിശോധനയിൽ, കുറഞ്ഞത് 2 വരികളെങ്കിലും കുറയുന്നു
- എഎംഡി കേസുകളിൽ 85-90 ശതമാനം വരുന്ന ഡ്രൈ മാക്കുലാർ ഡീജനറേഷനിൽ, ഫണ്ടസ് ഫോട്ടോഗ്രാഫിയിൽ ഡ്രൂസൻ പാടുകൾ കാണാം.
- ഒരു ഇലക്ട്രോറെറ്റിനോഗ്രാം ഉപയോഗിച്ച്, സാധാരണ കണ്ണുമായി താരതമ്യപ്പെടുത്തുമ്പോൾ ദുർബലമായ അല്ലെങ്കിൽ പ്രതികരണമില്ലാത്ത മാക്കുലയിലെ പോയിന്റുകൾ കണ്ടെത്താം
- കളർ അക്വിറ്റി, കളർ കോൺട്രാസ്റ്റ് സെൻസിറ്റിവിറ്റി എന്നിവ വിലയിരുത്തുന്നതിനായി ഫാർൺസ്വർത്ത്-മൺസെൽ 100 ഹ്യൂ ടെസ്റ്റ്, മാക്സിമം കളർ കോൺട്രാസ്റ്റ് സെൻസിറ്റിവിറ്റി ടെസ്റ്റ് (എംസിസിഎസ്) എന്നിവ ഉപയോഗിക്കാം
- രോഗനിർണയത്തിലും ആൻറി ആൻജിയോജനിക് മരുന്നുകളുമായുള്ള ചികിത്സയ്ക്കുള്ള പ്രതികരണത്തിന്റെ തുടർന്നുള്ള വിലയിരുത്തലിലും ഒപ്റ്റിക്കൽ കോഹെറൻസ് ടോമോഗ്രാഫി ഇപ്പോൾ മിക്ക നേത്രരോഗവിദഗ്ദ്ധരും ഉപയോഗിക്കുന്നു.
വെറ്റ് (അല്ലെങ്കിൽ അവസാന ഘട്ടത്തിൽ) എഎംഡിയുടെ രോഗനിർണയത്തിൽ മുകളിൽ പറഞ്ഞ പരിശോധനകൾക്ക് പുറമേ ഇനിപ്പറയുന്നവ കൂടി ഉൾപ്പെടാം:
- പ്രിഫറൻഷ്യൽ ഹൈപ്പർഅക്യുറ്റി പെരിമെട്രി മാറ്റങ്ങൾ (നനഞ്ഞ എഎംഡിക്ക്). കാഴ്ചയിലെ ഗുരുതരമായ മാറ്റങ്ങൾ കണ്ടെത്തുന്ന ഒരു പരിശോധനയാണ് പ്രിഫറൻഷ്യൽ ഹൈപ്പർക്യുറ്റി പെരിമെട്രി, വികൃതമായ ഡോട്ടുകളുടെ പാറ്റേണുകൾ ഉപയോഗിച്ച് മാക്യുലയെ ഉത്തേജിപ്പിക്കുകയും വിഷ്വൽ ഫീൽഡിൽ ഇത് എവിടെയാണ് സംഭവിക്കുന്നതെന്ന് രോഗി തിരിച്ചറിയുകയും ചെയ്യുന്നു.[54]
- വെറ്റ് മാക്കുലാർ ഡീജനറേഷനിൽ, മാക്യുലയ്ക്ക് പിന്നിലെ രക്തപ്രവാഹം നിരീക്ഷിക്കാൻ ആൻജിയോഗ്രാഫിക്ക് കഴിയും. അസാധാരണമായ വാസ്കുലർ പ്രോസസുകളെ തിരിച്ചറിയാനും പ്രാദേശികവൽക്കരിക്കാനും ഫ്ലൂറസെൻ ആൻജിയോഗ്രാഫി അനുവദിക്കുന്നു.
ഹിസ്റ്റോളജി[തിരുത്തുക]
- റെറ്റിനയിലെ പിഗ്മെന്ററി മാറ്റങ്ങൾ - ഐറിസിലെ പിഗ്മെന്റ് കോശങ്ങൾക്ക് പുറമേ (കണ്ണിന്റെ നിറമുള്ള ഭാഗം), റെറ്റിനയ്ക്ക് ചുവടെ പിഗ്മെന്റ് കോശങ്ങളുണ്ട്. ഈ കോശങ്ങൾ തകർന്ന് അവയുടെ പിഗ്മെൻറ് നഷ്ടപ്പെട്ട്, പിന്നീട്, പിഗ്മെന്റ് കുറവുള്ള പ്രദേശങ്ങൾ പ്രത്യക്ഷപ്പെടാം
- എക്സുഡേറ്റീവ് മാറ്റങ്ങൾ: കണ്ണിലെ രക്തസ്രാവം, ഹാർഡ് എക്സുഡേറ്റുകൾ, സബ്റെറ്റിനൽ / സബ്-ആർപിഇ / ഇൻട്രാറെറ്റിനൽ ദ്രാവകം
- ഡ്രൂസെൻ, റെറ്റിനയിൽ കെട്ടിപ്പടുക്കുന്ന എക്സ്ട്രാ സെല്ലുലാർ വസ്തുക്കളുടെ ചെറിയ ശേഖരണം. കാഴ്ചയുടെ പുരോഗതി നഷ്ടപ്പെടുന്നതിന് ഡ്രൂസനെ കുറ്റപ്പെടുത്തുന്ന പ്രവണതയുണ്ടെങ്കിലും, കാഴ്ച നഷ്ടപ്പെടാതെ ഡ്രൂസൻ നിക്ഷേപം റെറ്റിനയിൽ ഉണ്ടാകാം. ഡ്രൂസന്റെ വലിയ നിക്ഷേപമുള്ള ചില രോഗികൾക്ക് സാധാരണ വിഷ്വൽ അക്വിറ്റി ഉണ്ട്. ഉയർന്ന സാന്ദ്രത ഡ്രൂസൻ ഉള്ളപ്പോൾ റെറ്റിനയിൽ സാധാരണ റെറ്റിന റിസപ്ഷനും ഇമേജ് ട്രാൻസ്മിഷനും സാധ്യമാണെങ്കിൽ, വിഷ്വൽ ഫംഗ്ഷൻ നഷ്ടപ്പെടുന്നതിന് ഡ്രൂസനെ ഉൾപ്പെടുത്താമെങ്കിലും, കാഴ്ച നഷ്ടപ്പെടുന്നതിന് മറ്റൊരു ഘടകമെങ്കിലും ഉണ്ടായിരിക്കണം .
പ്രതിരോധം[തിരുത്തുക]
2017 ലെ കോക്രൺ അവലോകനത്തിൽ വിറ്റാമിൻ, മിനറൽ സപ്ലിമെന്റുകൾ ഒറ്റയ്ക്കോ കൂട്ടായോ ഉപയോഗിക്കുന്നത് സാധാരണ ജനങ്ങൾക്ക് എഎംഡി ഉണ്ടോ ഇല്ലയോ എന്നതിനെ ബാധിക്കുന്നില്ലെന്ന് കണ്ടെത്തി.[4]
ചികിത്സ[തിരുത്തുക]
രോഗത്തിന്റെ തരത്തെ ആശ്രയിച്ച് എഎംഡിയുടെ ചികിത്സ വ്യത്യാസപ്പെടുന്നു. പൊതുവേ, എഎംഡിയുടെ പുരോഗതി മന്ദഗതിയിലാക്കുകയാണ് ചികിത്സയുടെ പ്രധാന ലക്ഷ്യം.[55] 2018 ലെ കണക്കനുസരിച്ച്, എഎംഡിയുടെ ഫലങ്ങൾ മാറ്റുന്നതിനുള്ള ചികിത്സകളൊന്നുമില്ല. അറിയപ്പെടുന്ന അപകടസാധ്യത ഘടകങ്ങളായ പുകവലി, രക്തപ്രവാഹത്തിന് മാറ്റം വരുത്തുക, ഭക്ഷണത്തിൽ മാറ്റങ്ങൾ വരുത്തുക എന്നിവയിലൂടെയാണ് ആദ്യഘട്ടവും ഇന്റർമീഡിയറ്റ്-സ്റ്റേജ് എഎംഡിയും നിയന്ത്രിക്കുന്നത്. ഇന്റർമീഡിയറ്റ്-സ്റ്റേജ് എഎംഡി മാനേജ്മെൻറിൽ ആന്റിഓക്സിഡന്റും മിനറൽ സപ്ലിമെന്റേഷനും ഉൾപ്പെടുന്നു.[56] കോറോയിഡൽ നിയോവാസ്കുലറൈസേഷന്റെ (സിഎൻവി) സാന്നിധ്യം അടിസ്ഥാനമാക്കിയാണ് അഡ്വാൻസ്ഡ്-സ്റ്റേജ് എഎംഡി കൈകാര്യം ചെയ്യുന്നത്: ഡ്രൈ എഎംഡി (സിഎൻവി നിലവിലില്ല) അല്ലെങ്കിൽ വെറ്റ് എഎംഡി (സിഎൻവി നിലവിലുണ്ട്). ഡ്രൈ എഎംഡിക്ക് ഫലപ്രദമായ ചികിത്സകളൊന്നും നിലവിലില്ല. വെറ്റ് എഎംഡിയിലുള്ള സിഎൻവി നിയന്ത്രിക്കുന്നത് വാസ്കുലർ എൻഡോ തീലിയൽ ഗ്രോത്ത് ഫാക്ടർ (വിഇജിഎഫ്) ഇൻഹിബിറ്ററുകളാണ്.[57] [58]
ഡ്രൈ എഎംഡി[തിരുത്തുക]
ഈ അവസ്ഥയ്ക്ക് മെഡിക്കൽ അല്ലെങ്കിൽ ശസ്ത്രക്രിയാ ചികിത്സ ലഭ്യമല്ല.
വെറ്റ് എഎംഡി[തിരുത്തുക]
വെറ്റ് എഎംഡിയിലെ സിഎൻവി ചികിത്സയ്ക്കായി റാനിബിസുമാബ്, അഫ്ലിബെർസെപ്റ്റ്, ബ്രോലുസിസുമാബ് എന്നീ വിഇജിഎഫ് ഇൻഹിബിറ്ററുകൾ അംഗീകരിച്ചിട്ടുണ്ട്.[57] [59] മൂന്ന് മരുന്നുകളും ഇൻട്രാവിട്രിയൽ കുത്തിവയ്പ്പിലൂടെയാണ് നൽകുന്നത്, അതായത് അവ നേരിട്ട് കണ്ണിലേക്ക് കുത്തിവയ്ക്കുന്നു. മുമ്പത്തെ രണ്ട് മരുന്നുകളുടേതിന് സമാനമായ ഫലപ്രാപ്തിയും സുരക്ഷയും ഉണ്ടെന്ന് തെളിയിക്കപ്പെട്ടിട്ടുള്ള മറ്റൊരു വിഇജിഎഫ് ഇൻഹിബിറ്ററാണ് ബെവാസിസുമാബ്, എന്നിരുന്നാലും ഇത് നിലവിൽ എഎംഡിക്ക് സൂചിപ്പിച്ചിട്ടില്ല. [58] ലേസർ കോയാഗ്യുലേഷൻ തെറാപ്പി ഉപയോഗിച്ചും എഎംഡി ചികിത്സിക്കാം.[60]
ക്രമരഹിതമായ ഒരു നിയന്ത്രിത ട്രയലിൽ ബെവാസിസുമാബിനും റാണിബിസുമാബിനും സമാനമായ ഫലപ്രാപ്തി ഉണ്ടെന്ന് കണ്ടെത്തി.[61] ഗ്യാസ്ട്രോഇന്റസ്റ്റൈനൽ ഡിസോർഡേഴ്സ് ഒഴികെ നിയോവാസ്കുലർ എഎംഡി ചികിത്സിക്കാൻ ഉപയോഗിക്കുമ്പോൾ ബെവാസിസുമാബിന്റെയും റാണിബിസുമാബിന്റെയും വ്യവസ്ഥാപരമായ സുരക്ഷ സമാനമാണെന്ന് 2014 ലെ ഒരു കോക്രൺ അവലോകനത്തിൽ കണ്ടെത്തി.[62] എന്നിരുന്നാലും മാക്യുലർ ഡീജനറേഷൻ ചികിത്സയ്ക്കായി ബെവാസിസുമാബ് എഫ്ഡിഎ അംഗീകരിച്ചിട്ടില്ല. അംഗീകൃതവും എന്നാൽ ചെലവേറിയതുമായ റാണിബിസുമാബിനെക്കാൾ വിലകുറഞ്ഞ ബെവാസിസുമാബിന്റെ ഓഫ്-ലേബൽ ഉപയോഗം യുകെയിലെ ഒരു വിവാദത്തിൽ ഉൾപ്പെടുന്നു. കണ്ണ് കുത്തിവയ്പ്പുകൾക്കായി പ്രത്യേകം രൂപകൽപ്പന ചെയ്ത പാരന്റ് ബെവാസിസുമാബ് തന്മാത്രയുടെ ഫാബ് ശകലമാണ് റാണിബിസുമാബ്. നിയോ വാസ്കുലർ എഎംഡിയുടെ ചികിത്സയ്ക്കായി അംഗീകരിച്ച മറ്റ് ആൻറി ആൻജിയോജനിക് മരുന്നുകളിൽ പെഗപ്റ്റാനിബ്[63], അഫ്ലിബെർസെപ്റ്റ് എന്നിവ ഉൾപ്പെടുന്നു.
അമേരിക്കൻ അക്കാദമി ഓഫ് ഒഫ്താൽമോളജി പ്രാക്ടീസ് മാർഗ്ഗനിർദ്ദേശങ്ങൾ മാക്യുലർ ഡീജനറേഷനായി ലേസർ കോയാഗ്യുലേഷൻ തെറാപ്പി ശുപാർശ ചെയ്യുന്നില്ല, പക്ഷേ മരുന്ന് ചികിത്സയോട് പ്രതികരിക്കാത്ത, ഫോവിയയ്ക്ക് പുറത്തുള്ള കോറോയിഡിൽ പുതിയ രക്തക്കുഴലുകളുള്ള ആളുകൾക്ക് ഇത് ഉപയോഗപ്രദമാകുമെന്ന് പ്രസ്താവിക്കുന്നു.[64] [65] ലേസർ കൊയാഗുലേഷൻ ഡ്രൂസൻ മാഞ്ഞുപോകുന്നതിന് കാരണമാകുമെന്നതിന് ശക്തമായ തെളിവുകളുണ്ട്, പക്ഷേ ഇത് കോറോയ്ഡൽ നിയോവാസ്കുലറൈസേഷനെ ബാധിക്കില്ല.[66] 2007 ലെ കോക്രൺ അവലോകനത്തിൽ, ഫൊവിയയ്ക്ക് പുറത്തുള്ള കോറോയിഡിലെ പുതിയ രക്തക്കുഴലുകളുടെ ലേസർ ഫോട്ടോകോയാഗുലേഷൻ ഫലപ്രദവും സാമ്പത്തികവുമായ രീതിയാണെന്ന് കണ്ടെത്തി, പക്ഷേ ഇത് ഫോവിയയ്ക്ക് അടുത്തോ താഴെയോ ഉള്ള രക്തകുഴലുകൾക്ക് മാത്രമായി പരിമിതപ്പെടുത്തിയിരിക്കുന്നു.[67]
വെറ്റ് എഎംഡിയെ ചികിത്സിക്കാൻ ഫോട്ടോഡൈനാമിക് തെറാപ്പിയും ഉപയോഗിച്ചുവരുന്നുണ്ട്.[68] മരുന്ന് വെർട്ടെപോർഫിൻ ഞരമ്പിലൂടെയാണ് നൽകുന്നത്; അതിനുശേഷം ഒരു പ്രത്യേക തരംഗദൈർഘ്യത്തിന്റെ പ്രകാശം അസാധാരണ രക്തക്കുഴലുകളിൽ പ്രയോഗിക്കുന്നു. ഇത് വെർട്ടെപോർഫിൻ സജീവമാക്കി രക്തകുഴലുകളെ നശിപ്പിക്കുന്നു.
തിമിര ശസ്ത്രക്രിയ എഎംഡിയുള്ള ആളുകൾക്ക് വിഷ്വൽ ഫലങ്ങൾ മെച്ചപ്പെടുത്താൻ കഴിയും, എഎംഡിയുടെ പുരോഗതി വർദ്ധിപ്പിക്കുന്ന ശസ്ത്രക്രിയയെക്കുറിച്ച് ആശങ്കകളുണ്ടെങ്കിലും. ക്രമരഹിതമായ നിയന്ത്രിത ട്രയലിൽ, തിമിര ശസ്ത്രക്രിയയ്ക്ക് വിധേയരായ ആളുകൾക്ക് (രണ്ടാഴ്ചയ്ക്കുള്ളിൽ) വൈകിയ തിമിര ശസ്ത്രക്രിയയ്ക്ക് വിധേയരായവരേക്കാൾ (6 മാസം) കാഴ്ചശക്തിയും ജീവിത ഫലങ്ങളുടെ ഗുണനിലവാരവും മെച്ചപ്പെട്ടതായി കണ്ടെത്തിയിട്ടുണ്ട്.[69]
അഡാപ്റ്റീവ് ഉപകരണങ്ങൾ[തിരുത്തുക]

പെരിഫറൽ കാഴ്ചയെ ബാധിക്കാത്തതിനാൽ, മാക്യുലർ ഡീജനറേഷൻ ഉള്ള ആളുകൾക്ക് അവരുടെ കാഴ്ച ഭാഗികമായി ശരിയാക്കാൻ, പെരിഫറൽ കാഴ്ച ഉപയോഗിക്കാൻ ശീലിക്കുന്നതിലൂടെ കഴിയും.[70]
മാഗ്നിഫൈയിംഗ് ഗ്ലാസുകൾ, പ്രത്യേക കണ്ണട ലെൻസുകൾ, കമ്പ്യൂട്ടർ സ്ക്രീൻ റീഡറുകൾ, മെറ്റീരിയൽ വായന വിപുലീകരിക്കുന്ന ടിവി പോലെയുള്ള അഡാപ്റ്റീവ് ഉപകരണങ്ങൾ ആളുകളെ വായിക്കാൻ സഹായിക്കുന്നു. സംവിധാനങ്ങൾ എന്നിവ ഇതിൽ ഉൾപ്പെടുന്നു.
കമ്പ്യൂട്ടർ സ്ക്രീൻ റീഡറുകളായ JAWS അല്ലെങ്കിൽ തണ്ടർ സാധാരണ വിൻഡോസ് കമ്പ്യൂട്ടറുകളിൽ പ്രവർത്തിക്കുന്നു. കൂടാതെ, ആപ്പിൾ ഉപകരണങ്ങൾ വോയ്സ് ഓവർ, സ്ക്രീൻ റീഡറുകൾ, ബ്രെയ്ലി മുതലായ വൈവിധ്യമാർന്ന സവിശേഷതകൾ നൽകുന്നു.
വീഡിയോ ക്യാമറകൾ സ്റ്റാൻഡേർഡ് അല്ലെങ്കിൽ പ്രത്യേക-ഉദ്ദേശ്യ കമ്പ്യൂട്ടർ മോണിറ്ററുകളിലേക്ക് ചേർത്ത് ചിത്രം വലുതാക്കി നോക്കാൻ കഴിയും. ലിഖിത മെറ്റീരിയൽ നീക്കാൻ ചലിക്കുന്ന ടേബിളും ഈ സിസ്റ്റങ്ങളിൽ പലപ്പോഴും ഉൾപ്പെടുന്നു.
വലിയ ഫോണ്ടുകൾ ഉള്ള പുസ്തകങ്ങൾ, ട്രാക്കിംഗ് എളുപ്പമാക്കുന്നതിനുള്ള പാറ്റേണുകൾ, വാചകവും ഓഡിയോയും ഉള്ള ഓഡിയോബുക്കുകൾ, ഡെയ്സി പുസ്തകങ്ങൾ എന്നിവയും കാഴ്ച കുറവ് ഉള്ളവർക്ക് വേണ്ടിയുണ്ട്.
എപ്പിഡെമോളജി[തിരുത്തുക]

ഏഷ്യക്കാരെയും ആഫ്രിക്കക്കാരെയും അപേക്ഷിച്ച് പ്രായവുമായി ബന്ധപ്പെട്ട ഏത് മാക്യുലർ ഡീജനറേഷനും യൂറോപ്പുകാരിൽ കൂടുതലാണ്.[72] ഏഷ്യക്കാരും ആഫ്രിക്കക്കാരും തമ്മിൽ കണക്കിൽ കാര്യമായ വ്യത്യാസമില്ല. പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷനും അതുമായി ബന്ധപ്പെട്ട സവിശേഷതകളും പ്രായത്തിനനുസരിച്ച് വർദ്ധിക്കുന്നതിനാൽ 55 വയസ്സിന് താഴെ പ്രായമുള്ള ആളുകളിൽ ഇത് കുറവാണ്.[73] രോഗ വർദ്ധനയുമായി ബന്ധപ്പെട്ട് പരിഷ്ക്കരിക്കാവുന്ന ഏറ്റവും ശക്തമായ ഘടകമാണ് പുകവലി.[74] യുഎസ്എയിലെ വെളുത്ത ജനസംഖ്യയിൽ കാഴ്ചശക്തി നഷ്ടപ്പെടുന്നതിന്റെ കാരണങ്ങളിൽ 54% ത്തിലധികവും പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷൻ മൂലം ആണ്. ഏകദേശം 8 ദശലക്ഷം അമേരിക്കക്കാരെ പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷൻ ബാധിക്കുന്നു, അവരിൽ 1 ദശലക്ഷത്തിലധികം പേർക്ക് അടുത്ത 5 വർഷത്തിനുള്ളിൽ പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷൻ തീവ്ര അവസ്ഥയിലാകും. യുകെയിൽ, 65–74 വയസ് പ്രായമുള്ളവരിൽ ഏകദേശം 42% നും, 75–84 വയസ് പ്രായമുള്ളവരിൽ മൂന്നിൽ രണ്ട് ഭാഗത്തിനും, 85 വയസ്സ് മുതൽ മുകളിലോട്ട് പ്രായമുള്ളവരിൽ മുക്കാൽ ഭാഗത്തിനും അന്ധതയ്ക്ക് കാരണമാകുന്നത് പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷനാണ്.
ഗവേഷണ നിർദ്ദേശങ്ങൾ[തിരുത്തുക]
പ്രായവുമായി ബന്ധപ്പെട്ട മറ്റ് രോഗങ്ങളുമായുള്ള ബന്ധം[തിരുത്തുക]
എഎംഡിയുമായി ബന്ധപ്പെട്ട ഡ്രൂസൻ, തന്മാത്രാ ഘടനയിൽ പ്രായവുമായി ബന്ധപ്പെട്ട മറ്റ് രോഗങ്ങളായ അൽഷിമേഴ്സ് രോഗം, ആർത്തെറോസ്ലീറോസിസ് പോലെയുള്ള രോഗാവസ്ഥകളിലെ ബീറ്റാ-അമിലോയിഡ് (βA) പ്ലേക്കുകൾക്കും ഡെപ്പോസിറ്റുകൾക്കും സമാനമാണെന്നും പഠനങ്ങൾ സൂചിപ്പിക്കുന്നു. എഎംഡിയുടെയും പ്രായവുമായി ബന്ധപ്പെട്ട മറ്റ് രോഗങ്ങളുടെയും കാരണങ്ങളിൽ സമാനമായ മാർഗങ്ങൾ ഉൾപ്പെട്ടിരിക്കാമെന്ന് ഇത് സൂചിപ്പിക്കുന്നു.[75]
ജനിതക പരിശോധന[തിരുത്തുക]
എഎംഡിയുമായി ബന്ധപ്പെട്ട ജനിതക മാർക്കറുകളുടെ ഒരു പ്രായോഗിക പ്രയോഗം എഎംഡിയുടെ രോഗത്തിൻറെ പ്രാരംഭ ഘട്ടത്തിൽ നിന്ന് നിയോവാസ്കുലറൈസേഷനിലേക്കുള്ള പുരോഗതി പ്രവചനത്ത്ന് സഹായകരമാവും.[41] [42]
സ്റ്റെം സെൽ ട്രാൻസ്പ്ലാൻറ്[തിരുത്തുക]
അസ്ഥി മജ്ജ സ്റ്റെം സെല്ലുകൾ ഉപയോഗിച്ചുള്ള സെൽ അധിഷ്ഠിത ചികിത്സകളും, റെറ്റിന പിഗ്മെന്റ് എപ്പിത്തീലിയൽ ട്രാൻസ്പ്ലാൻറേഷനും പഠനവിധേയമാക്കിയിട്ടുണ്ട്.[76] ഇതുമായി ബന്ധപ്പെട്ട് പ്രോത്സാഹജനകമായ ഫലങ്ങളുമായി മനുഷ്യരിൽ നിരവധി പരീക്ഷണങ്ങൾ നടന്നിട്ടുണ്ട്. [77]
മറ്റ് തരങ്ങൾ[തിരുത്തുക]
സമാനമായ ലക്ഷണങ്ങളുള്ള മറ്റ് ചില (അപൂർവ) തരം മാക്യുലർ ഡീജനറേഷൻ ഉണ്ട്, പക്ഷേ വെറ്റ് അല്ലെങ്കിൽ ഡ്രൈ മാക്കുലാർ ഡീജനറേഷനുമായി എറ്റിയോളജിക്കലി ഇവയ്ക്ക് ബന്ധമില്ല. കുട്ടിക്കാലത്തോ മധ്യവയസ്സിലോ ഉണ്ടാകാവുന്ന ജനിതക വൈകല്യങ്ങളാണ് അവയെല്ലാം.
- വിറ്റെല്ലിഫോം മാക്കുലാർ ഡിസ്ട്രോഫി
- സോർസ്ബിസ് ഫണ്ടസ് ഡിസ്ട്രോഫി: ഇത് ചികിത്സിക്കാൻ കഴിയാത്ത സബ് മാക്യുലർ നിയോവാസ്കുലറൈസേഷന്റെ ഫലമായുണ്ടാകുന്ന, പെട്ടെന്നുള്ള കാഴ്ച നഷ്ടം ലക്ഷണമായുള്ള, ഒരു ഓട്ടോസോമൽ ഡോമിനൻ്റ് റെറ്റിന രോഗമാണ്
- ജുവനൈൽ-ഓൺസെറ്റ് മാക്കുലാർ ഡിസ്ട്രോഫി: പെരിഫറൽ റെറ്റിനയിലെ മാറ്റങ്ങൾ, ലിപ്പോഫുസിൻ പോലുള്ള വസ്തുക്കളുടെ സബ്റെറ്റിനൽ ഡിപോസിഷൻ, എന്നിവയുടെ സവിശേഷതകളുള്ള ഒരു ഓട്ടോസോമൽ റിസസിവ് റെറ്റിനൽ ഡിസോർഡറാണ് സ്റ്റാർഗാർഡ്റ്റ് രോഗം (ജുവനൈൽ മാക്കുലാർ ഡീജനറേഷൻ, എസ്ടിജിഡി).
വളരെ വ്യത്യസ്തമായ എറ്റിയോളജിയും വ്യത്യസ്ത ചികിത്സയും ഉള്ള, എപിറെറ്റിനൽ മെംബ്രൺ (മാക്യുലാർ പക്കർ), സെൻട്രൽ സീറസ് റെറ്റിനോപ്പതി പോലുള്ള മാക്കുലയെ ബാധിക്കുന്ന മറ്റ് അവസ്ഥകളിലും സമാന ലക്ഷണങ്ങൾ ഉണ്ടാകാം.
ശ്രദ്ധേയമായ കേസുകൾ[തിരുത്തുക]
പരാമർശങ്ങൾ[തിരുത്തുക]
- ↑ 1.00 1.01 1.02 1.03 1.04 1.05 1.06 1.07 1.08 1.09 1.10 1.11 1.12 1.13 1.14 1.15 1.16 "Facts About Age-Related Macular Degeneration". National Eye Institute. June 2015. Archived from the original on 22 December 2015. Retrieved 21 December 2015.
- ↑ 2.0 2.1 GBD 2015 Disease and Injury Incidence and Prevalence Collaborators (October 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015". The Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577. PMID 27733282.
{{cite journal}}:|last=has generic name (help)CS1 maint: numeric names: authors list (link) - ↑ 3.0 3.1 "Age-Related Macular Degeneration". Primary Care. 42 (3): 377–91. September 2015. doi:10.1016/j.pop.2015.05.009. PMID 26319344.
- ↑ 4.0 4.1 "Antioxidant vitamin and mineral supplements for preventing age-related macular degeneration". The Cochrane Database of Systematic Reviews. 7: CD000253. July 2017. doi:10.1002/14651858.CD000253.pub4. PMC 6483250. PMID 28756617.
- ↑ "Antioxidant vitamin and mineral supplements for slowing the progression of age-related macular degeneration". The Cochrane Database of Systematic Reviews. 7: CD000254. July 2017. doi:10.1002/14651858.CD000254.pub4. PMC 6483465. PMID 28756618.
- ↑ Vos, Theo; Barber, Ryan M.; Bell, Brad; Bertozzi-Villa, Amelia; Biryukov, Stan; Bolliger, Ian; Charlson, Fiona; Davis, Adrian; Degenhardt, Louisa (August 2015). "Global, regional, and national incidence, prevalence, and years lived with disability for 301 acute and chronic diseases and injuries in 188 countries, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013". The Lancet. 386 (9995): 743–800. doi:10.1016/s0140-6736(15)60692-4. PMC 4561509. PMID 26063472.
{{cite journal}}: Invalid|display-authors=29(help) - ↑ "Wayback Machine". 22 October 2013. Retrieved 5 November 2018.
- ↑ Roberts, DL (September 2006). "The First Year – Age Related Macular Degeneration". Marlowe & Company: 100.
- ↑ Roberts, DL (September 2006). "The First Year – Age Related Macular Degeneration". Marlowe & Company: 20.
- ↑ "Recognizing age-related macular degeneration in primary care". JAAPA. 30 (3): 18–22. March 2017. doi:10.1097/01.jaa.0000512227.85313.05. PMID 28151737.
- ↑ 11.0 11.1 "Age-related macular degeneration". The Lancet. 379 (9827): 1728–38. May 2012. doi:10.1016/S0140-6736(12)60282-7. PMID 22559899.
- ↑ "Genetics of age-related macular degeneration: current concepts, future directions". Seminars in Ophthalmology. 26 (3): 77–93. May 2011. doi:10.3109/08820538.2011.577129. PMC 4242505. PMID 21609220.
- ↑ 13.0 13.1 "Smoking and age-related macular degeneration: a review of association". Eye. 19 (9): 935–44. September 2005. doi:10.1038/sj.eye.6701978. PMID 16151432.
- ↑ "Long-term blood pressure and age-related macular degeneration: the ALIENOR study". Investigative Ophthalmology & Visual Science. 54 (3): 1905–12. March 2013. doi:10.1167/iovs.12-10192. PMID 23404120.
{{cite journal}}: Invalid|display-authors=6(help) - ↑ "Early and intermediate age-related macular degeneration: update and clinical review". Clinical Interventions in Aging. 12: 1579–1587. October 2017. doi:10.2147/cia.s142685. PMC 5633280. PMID 29042759.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ↑ "Cholesterol-enriched diet causes age-related macular degeneration-like pathology in rabbit retina". BMC Ophthalmology. 11: 22. August 2011. doi:10.1186/1471-2415-11-22. PMC 3170645. PMID 21851605.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ↑ "Abdominal obesity and age-related macular degeneration". American Journal of Epidemiology. 173 (11): 1246–55. June 2011. doi:10.1093/aje/kwr005. PMID 21422060.
- ↑ "Association between dietary fat intake and age-related macular degeneration in the Carotenoids in Age-Related Eye Disease Study (CAREDS): an ancillary study of the Women's Health Initiative". Archives of Ophthalmology. 127 (11): 1483–93. November 2009. doi:10.1001/archophthalmol.2009.130. PMC 3144752. PMID 19901214.
{{cite journal}}: Invalid|display-authors=6(help) - ↑ "The relationship of dietary lipid intake and age-related macular degeneration in a case-control study: AREDS Report No. 20". Archives of Ophthalmology. 125 (5): 671–9. May 2007. doi:10.1001/archopht.125.5.671. PMID 17502507.
{{cite journal}}: Invalid|display-authors=6(help) - ↑ "What do we know about the macular pigment in AMD: the past, the present, and the future". Eye. 32 (5): 992–1004. May 2018. doi:10.1038/s41433-018-0044-0. PMC 5944649. PMID 29576617.
- ↑ "Are Computer Glasses Worth It?". American Academy of Ophthalmology. 2017-04-27. Retrieved 2020-02-02.
- ↑ "Common variation in three genes, including a noncoding variant in CFH, strongly influences risk of age-related macular degeneration". Nature Genetics. 38 (9): 1055–9. September 2006. doi:10.1038/ng1873. PMID 16936732.
- ↑ "Complement factor H polymorphism and age-related macular degeneration". Science. 308 (5720): 421–4. April 2005. Bibcode:2005Sci...308..421E. doi:10.1126/science.1110189. PMID 15761121.
- ↑ "A common CFH haplotype, with deletion of CFHR1 and CFHR3, is associated with lower risk of age-related macular degeneration". Nature Genetics. 38 (10): 1173–7. October 2006. doi:10.1038/ng1890. PMID 16998489.
- ↑ "An imbalance of human complement regulatory proteins CFHR1, CFHR3 and factor H influences risk for age-related macular degeneration (AMD)". Human Molecular Genetics. 19 (23): 4694–704. December 2010. doi:10.1093/hmg/ddq399. PMID 20843825.
{{cite journal}}: Invalid|display-authors=6(help) - ↑ "Complement C3 variant and the risk of age-related macular degeneration". The New England Journal of Medicine. 357 (6): 553–61. August 2007. doi:10.1056/NEJMoa072618. PMID 17634448.
{{cite journal}}: Invalid|display-authors=6(help) - ↑ "Variation in complement factor 3 is associated with risk of age-related macular degeneration". Nature Genetics. 39 (10): 1200–1. October 2007. doi:10.1038/ng2131. PMID 17767156.
- ↑ "A variant of the HTRA1 gene increases susceptibility to age-related macular degeneration". Science. 314 (5801): 992–3. November 2006. Bibcode:2006Sci...314..992Y. doi:10.1126/science.1133811. PMID 17053109.
{{cite journal}}: Invalid|display-authors=6(help) - ↑ "HTRA1 promoter polymorphism in wet age-related macular degeneration". Science. 314 (5801): 989–92. November 2006. Bibcode:2006Sci...314..989D. doi:10.1126/science.1133807. PMID 17053108.
- ↑ "Mitochondrial DNA haplogroups associated with age-related macular degeneration". Investigative Ophthalmology & Visual Science. 50 (6): 2966–74. June 2009. doi:10.1167/iovs.08-2646. PMID 19151382.
- ↑ "Drusen associated with aging and age-related macular degeneration contain proteins common to extracellular deposits associated with atherosclerosis, elastosis, amyloidosis, and dense deposit disease". FASEB Journal. 14 (7): 835–46. May 2000. doi:10.1096/fasebj.14.7.835. PMID 10783137.
- ↑ "A common haplotype in the complement regulatory gene factor H (HF1/CFH) predisposes individuals to age-related macular degeneration". Proceedings of the National Academy of Sciences of the United States of America. 102 (20): 7227–32. May 2005. doi:10.1073/pnas.0501536102. PMC 1088171. PMID 15870199.
{{cite journal}}: Invalid|display-authors=6(help) - ↑ "Association of complement factor H polymorphisms with exudative age-related macular degeneration". Molecular Vision. 12: 1536–42. December 2006. PMID 17167412.
- ↑ "Complement factor H polymorphism, complement activators, and risk of age-related macular degeneration". JAMA. 296 (3): 301–9. July 2006. doi:10.1001/jama.296.3.301. PMID 16849663.
- ↑ "CFH haplotypes without the Y402H coding variant show strong association with susceptibility to age-related macular degeneration". Nature Genetics. 38 (9): 1049–54. September 2006. doi:10.1038/ng1871. PMC 1941700. PMID 16936733.
{{cite journal}}: Invalid|display-authors=6(help) - ↑ "Complement factor H variant increases the risk of age-related macular degeneration". Science. 308 (5720): 419–21. April 2005. Bibcode:2005Sci...308..419H. doi:10.1126/science.1110359. PMID 15761120.
- ↑ Rohrer, Bärbel; Long, Qin; Coughlin, Beth; Renner, Brandon; Huang, Yuxiang; Kunchithapautham, Kannan; Ferreira, Viviana P.; Pangburn, Michael K.; Gilkeson, Gary S. (2010). "A Targeted Inhibitor of the Complement Alternative Pathway Reduces RPE Injury and Angiogenesis in Models of Age-Related Macular Degeneration". Inflammation and Retinal Disease: Complement Biology and Pathology. Advances in Experimental Medicine and Biology. Vol. 703. pp. 137–149. doi:10.1007/978-1-4419-5635-4_10. ISBN 978-1-4419-5634-7. PMID 20711712.
- ↑ "Sublytic membrane-attack-complex (MAC) activation alters regulated rather than constitutive vascular endothelial growth factor (VEGF) secretion in retinal pigment epithelium monolayers". The Journal of Biological Chemistry. 286 (27): 23717–24. July 2011. doi:10.1074/jbc.M110.214593. PMC 3129152. PMID 21566137.
- ↑ Yates, John R.W.; Sepp, Tiina; Matharu, Baljinder K.; Khan, Jane C.; Thurlby, Deborah A.; Shahid, Humma; Clayton, David G.; Hayward, Caroline; Morgan, Joanne (9 August 2007). "Complement C3 Variant and the Risk of Age-Related Macular Degeneration". New England Journal of Medicine. 357 (6): 553–561. doi:10.1056/NEJMoa072618. PMID 17634448.
- ↑ Fritsche LG, Loenhardt T, Janssen A, Fisher SA, Rivera A, Keilhauer CN, Weber BH (July 2008). "Age-related macular degeneration is associated with an unstable ARMS2 (LOC387715) mRNA". Nature Genetics. 40 (7): 892–6. doi:10.1038/ng.170. PMID 18511946.
- ↑ 41.0 41.1 "Genetic variants near TIMP3 and high-density lipoprotein-associated loci influence susceptibility to age-related macular degeneration". Proceedings of the National Academy of Sciences of the United States of America. 107 (16): 7401–6. April 2010. Bibcode:2010PNAS..107.7401C. doi:10.1073/pnas.0912702107. PMC 2867722. PMID 20385819.
{{cite journal}}: Invalid|display-authors=6(help) - ↑ 42.0 42.1 "Genome-wide association study of advanced age-related macular degeneration identifies a role of the hepatic lipase gene (LIPC)". Proceedings of the National Academy of Sciences of the United States of America. 107 (16): 7395–400. April 2010. Bibcode:2010PNAS..107.7395N. doi:10.1073/pnas.0912019107. PMC 2867697. PMID 20385826.
- ↑ "Dementia of the eye: the role of amyloid beta in retinal degeneration". Eye. 29 (8): 1013–26. August 2015. doi:10.1038/eye.2015.100. PMC 4541342. PMID 26088679.
- ↑ 44.0 44.1 "Clinical classification of age-related macular degeneration". Ophthalmology. 120 (4): 844–51. April 2013. doi:10.1016/j.ophtha.2012.10.036. PMID 23332590.
- ↑ X. Shaw, Peter; Stiles, Travis; Douglas, Christopher; Ho, Daisy; Fan, Wei; Du, Hongjun; Xiao, Xu (2016). "Oxidative stress, innate immunity, and age-related macular degeneration". AIMS Molecular Science. 3 (2): 196–221. doi:10.3934/molsci.2016.2.196. PMC 4882104. PMID 27239555.
- ↑ Kauppinen, Anu; Paterno, Jussi J.; Blasiak, Janusz; Salminen, Antero; Kaarniranta, Kai (6 February 2016). "Inflammation and its role in age-related macular degeneration". Cellular and Molecular Life Sciences. 73 (9): 1765–1786. doi:10.1007/s00018-016-2147-8. PMC 4819943. PMID 26852158.
- ↑ Thulliez, Marie; Zhang, Qinqin; Shi, Yingying; Zhou, Hao; Chu, Zhongdi; de Sisternes, Luis; Durbin, Mary K.; Feuer, William; Gregori, Giovanni (June 2019). "Correlations between Choriocapillaris Flow Deficits around Geographic Atrophy and Enlargement Rates Based on Swept-Source OCT Imaging". Ophthalmology Retina. 3 (6): 478–488. doi:10.1016/j.oret.2019.01.024. PMID 31174669.
- ↑ Sarangarajan, Rangaprasad; Apte, Shireesh. P. (2005). "Melanin Aggregation and Polymerization: Possible Implications in Age-Related Macular Degeneration". Ophthalmic Research. 37 (3): 136–141. doi:10.1159/000085533. PMID 15867475.
- ↑ "Sunlight and the 10-year incidence of age-related maculopathy: the Beaver Dam Eye Study". Archives of Ophthalmology. 122 (5): 750–7. May 2004. doi:10.1001/archopht.122.5.750. PMID 15136324.
- ↑ "DNA damage and repair in age-related macular degeneration". Mutation Research. 669 (1–2): 169–76. October 2009. doi:10.1016/j.mrfmmm.2009.06.008. PMID 19559717.
- ↑ "Mitochondrial dysfunction in retinal diseases". Current Eye Research. 36 (12): 1069–77. December 2011. doi:10.3109/02713683.2011.607536. PMC 4516173. PMID 21978133.
- ↑ National Guideline Alliance (UK) (2018). Age-related macular degeneration: diagnosis and management. National Institute for Health and Care Excellence: Clinical Guidelines. London: National Institute for Health and Care Excellence (UK). ISBN 9781473127876. PMID 29400919.
- ↑ "Delayed Rod-Mediated Dark Adaptation Is a Functional Biomarker for Incident Early Age-Related Macular Degeneration". Ophthalmology. 123 (2): 344–51. February 2016. doi:10.1016/j.ophtha.2015.09.041. PMC 4724453. PMID 26522707.
- ↑ "Diagnostic accuracy of the Amsler grid and the preferential hyperacuity perimetry in the screening of patients with age-related macular degeneration: systematic review and meta-analysis". Eye. 28 (7): 788–96. July 2014. doi:10.1038/eye.2014.104. PMC 4094801. PMID 24788016.
- ↑ Bishop P. Age-related macular degeneration. BMJ Best Practice. 2018.
- ↑ "Antioxidant vitamin and mineral supplements for preventing age-related macular degeneration". The Cochrane Database of Systematic Reviews. 7: CD000253. July 2017. doi:10.1002/14651858.cd000253.pub4. PMC 6483250. PMID 28756617.
- ↑ 57.0 57.1 "Aflibercept for neovascular age-related macular degeneration". The Cochrane Database of Systematic Reviews. 2: CD011346. February 2016. doi:10.1002/14651858.cd011346.pub2. PMC 5030844. PMID 26857947.
- ↑ 58.0 58.1 "Omega 3 fatty acids for preventing or slowing the progression of age-related macular degeneration" (PDF). The Cochrane Database of Systematic Reviews (4): CD010015. April 2015. doi:10.1002/14651858.cd010015.pub3. PMID 25856365.
- ↑ Nguyen, Quan Dong. "Brolucizumab: Evolution through Preclinical and Clinical Studies and the Implications for the Management of Neovascular Age-Related Macular Degeneration". Opthalmology. doi:10.1016/j.ophtha.2019.12.031. PMID 32107066. Retrieved 17 March 2020.
- ↑ "Laser photocoagulation for neovascular age-related macular degeneration". The Cochrane Database of Systematic Reviews (3): CD004763. July 2007. doi:10.1002/14651858.cd004763.pub2. PMID 17636773.
- ↑ "Alternative treatments to inhibit VEGF in age-related choroidal neovascularisation: 2-year findings of the IVAN randomised controlled trial". The Lancet. 382 (9900): 1258–67. October 2013. doi:10.1016/S0140-6736(13)61501-9. PMID 23870813.
- ↑ "Systemic safety of bevacizumab versus ranibizumab for neovascular age-related macular degeneration". The Cochrane Database of Systematic Reviews. 9 (9): CD011230. September 2014. doi:10.1002/14651858.CD011230.pub2. PMC 4262120. PMID 25220133.
- ↑ "FDA Approves New Drug Treatment for Age-Related Macular Degeneration". FDA.gov. U.S. Food and Drug Administration. Archived from the original on 2015-11-20.
- ↑ "Age-Related Macular Degeneration PPP – Updated 2015". American Academy of Ophthalmology Preferred Practice Pattern. 29 January 2015. Archived from the original on 21 October 2016. Retrieved 22 October 2016.
- ↑ "Interventions for Age-Related Macular Degeneration: Are Practice Guidelines Based on Systematic Reviews?". Ophthalmology. 123 (4): 884–97. April 2016. doi:10.1016/j.ophtha.2015.12.004. PMC 4808456. PMID 26804762.
- ↑ "Laser treatment of drusen to prevent progression to advanced age-related macular degeneration". The Cochrane Database of Systematic Reviews. 10 (10): CD006537. October 2015. doi:10.1002/14651858.CD006537.pub3. PMC 4733883. PMID 26493180.
- ↑ "Laser photocoagulation for neovascular age-related macular degeneration". The Cochrane Database of Systematic Reviews (3): CD004763. July 2007. doi:10.1002/14651858.CD004763.pub2. PMID 17636773.
- ↑ Meads C (2003). "Clinical effectiveness and cost–utility of photodynamic therapy for wet age-related macular degeneration: a systematic review and economic evaluation". Health Technology Assessment. 7 (9): v–vi, 1–98. doi:10.3310/hta7090. PMID 12709292. Archived from the original on 2010-11-07.
- ↑ "Surgery for cataracts in people with age-related macular degeneration". The Cochrane Database of Systematic Reviews. 2: CD006757. February 2017. doi:10.1002/14651858.CD006757.pub4. PMC 3480178. PMID 28206671.
- ↑ "Low Vision Rehabilitation Delivery Model". Mdsupport.org. Archived from the original on 2010-11-07. Retrieved 2011-01-11.
- ↑ "WHO Disease and injury country estimates". World Health Organization. 2009. Archived from the original on 2009-11-11. Retrieved Nov 11, 2009.
- ↑ "Global prevalence of age-related macular degeneration and disease burden projection for 2020 and 2040: a systematic review and meta-analysis". The Lancet. Global Health. 2 (2): e106–16. February 2014. doi:10.1016/S2214-109X(13)70145-1. PMID 25104651.
- ↑ "Age-related macular degeneration - Symptoms, diagnosis and treatment". BMJ Best Practice. Retrieved 2018-11-13.
- ↑ "Smoking and age-related macular degeneration: review and update". Journal of Ophthalmology. 2013: 895147. 2013. doi:10.1155/2013/895147. PMC 3866712. PMID 24368940.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ↑ "Drusen associated with aging and age-related macular degeneration contain proteins common to extracellular deposits associated with atherosclerosis, elastosis, amyloidosis, and dense deposit disease". FASEB Journal. 14 (7): 835–46. May 2000. doi:10.1096/fasebj.14.7.835. PMID 10783137.
- ↑ "Choice of Cell Source in Cell-Based Therapies for Retinal Damage due to Age-Related Macular Degeneration: A Review". Journal of Ophthalmology. 2013: 1–9. 2013. doi:10.1155/2013/465169. PMC 3654320. PMID 23710332.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ↑ "Development of human embryonic stem cell therapies for age-related macular degeneration". Trends in Neurosciences. 36 (7): 385–95. July 2013. doi:10.1016/j.tins.2013.03.006. PMID 23601133.
- ↑ "Judi Dench 'can't read any more due to failing eyesight Archived 2020-11-12 at the Wayback Machine.", The Guardian, 23 February 2014
- ↑ "Joan bows out to a standing ovation Archived 2020-09-19 at the Wayback Machine.", The Guardian, 13 May 2014
- ↑ "Patrons of the Macular Society Archived 2013-02-08 at the Wayback Machine. ആർക്കൈവ് കോപ്പി വേ ബാക്ക് യന്ത്രത്തിൽ നിന്നും", Macular Society. (notable for doing the voice of Wallace from Wallace and Gromit until 2012)
പുറം കണ്ണികൾ[തിരുത്തുക]
| Classification | |
|---|---|
| External resources |
