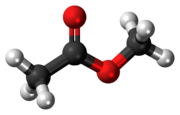
മീഥൈൽ അസറ്റേറ്റ്

| |
| |
| Names | |
|---|---|
| Preferred IUPAC name
Methyl acetate | |
| Systematic IUPAC name
Methyl ethanoate | |
| Other names
Methyl ester of acetic acid
| |
| Identifiers | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.001.078 |
| KEGG | |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| InChI | |
| SMILES | |
| Properties | |
| തന്മാത്രാ വാക്യം | |
| Molar mass | 0 g mol−1 |
| Appearance | Colorless liquid |
| Odor | Fragrant, fruity[2] |
| സാന്ദ്രത | 0.932 g cm−3 |
| ദ്രവണാങ്കം | |
| ക്വഥനാങ്കം | |
| ~25% (20 °C) | |
| ബാഷ്പമർദ്ദം | 173 mmHg (20°C)[2] |
| -42.60·10−6 cm3/mol | |
| Refractive index (nD) | 1.361 |
| Hazards | |
| Safety data sheet | External MSDS |
| Flash point | {{{value}}} |
| Explosive limits | 3.1%-16%[2] |
| Lethal dose or concentration (LD, LC): | |
LD50 (median dose)
|
3700 mg/kg (oral, rabbit)[3] |
LCLo (lowest published)
|
11,039 ppm (mouse, 4 hr) 21,753 ppm (cat, 1 hr) 32,000 ppm (rat, 4 hr)[3] |
| NIOSH (US health exposure limits): | |
PEL (Permissible)
|
TWA 200 ppm (610 mg/m3)[2] |
REL (Recommended)
|
TWA 200 ppm (610 mg/m3) ST 250 ppm (760 mg/m3)[2] |
IDLH (Immediate danger)
|
3100 ppm[2] |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
CH3COOCH3 എന്ന തന്മാത്രാസൂത്രമുള്ള ഒരു കാർബോക്സൈലേറ്റ് എസ്റ്ററാണ് മീഥൈൽ അസറ്റേറ്റ്. MeOAc, അസറ്റിക് ആസിഡ് മെഥൈൽ എസ്റ്റർ അല്ലെങ്കിൽ മെഥൈൽ എത്തനോയേറ്റ് എന്നീ പേരുകളിലും ഇത് അറിയപ്പെടുന്നു. ചില പശകളേയും നെയിൽ പോളിഷ് റിമൂവറുകളെയും അനുസ്മരിപ്പിക്കുന്ന മണം ഉള്ള കത്തുന്ന ദ്രാവകമാണിത്. സാധാരണ ഊഷ്മാവിൽ മെഥൈൽ അസറ്റേറ്റിന് വെള്ളത്തിൽ 25% ലേയത്വമുണ്ട് . ഉയർന്ന താപനിലയിൽ വെള്ളത്തിൽ അതിന്റെ ലായകത വളരെ കൂടുതലാണ്. ശക്തമായ ജലീയ ക്ഷാരത്തിന്റെയോ ജലീയ അമ്ലങ്ങളുടേയോ സാന്നിധ്യത്തിൽ മെഥൈൽ അസറ്റേറ്റ് സ്ഥിരതയുള്ളതല്ല.[4] [5]
തയ്യാറാക്കലും പ്രതികരണങ്ങളും
[തിരുത്തുക]അസറ്റിക് ആസിഡിന്റെ ഉൽപാദനത്തിന്റെ ഉപോൽപ്പന്നമായി മെഥനോൾ കാർബണിലേഷൻ വഴി മെഥൈൽ അസറ്റേറ്റ് വ്യാവസായികമായി ഉത്പാദിപ്പിക്കപ്പെടുന്നു. [6] സൾഫ്യൂറിക് ആസിഡ് പോലുള്ള ശക്തമായ ആസിഡുകളുടെ സാന്നിധ്യത്തിൽ മെഥനോൾ ഉപയോഗിച്ച് അസറ്റിക് ആസിഡ് എസ്റ്ററിഫിക്കേഷൻ വഴിയും മെഥൈൽ അസറ്റേറ്റ് ഉണ്ടാകുന്നു. റിയാക്ടീവ് ഡിസ്റ്റിലേഷൻ ഉപയോഗിച്ചുള്ള ഈ പ്രക്രിയ പ്രസിദ്ധമാണ്.
പ്രതികരണങ്ങൾ
[തിരുത്തുക]സോഡിയം ഹൈഡ്രോക്സൈഡ് അല്ലെങ്കിൽ ഹൈഡ്രോക്ലോറിക് ആസിഡ് അല്ലെങ്കിൽ സൾഫ്യൂറിക് ആസിഡ് പോലുള്ള ശക്തമായ ആസിഡുകളുടെ സാന്നിധ്യത്തിൽ, പ്രത്യേകിച്ചും ഉയർന്ന താപനിലയിൽ, ഇത് ഹൈഡ്രോളിസിസ് നടന്ന് വീണ്ടും മെഥനോൾ, അസറ്റിക് ആസിഡ് എന്നിവയാവുന്നു.
ഉപയോഗങ്ങൾ
[തിരുത്തുക]പശ, പെയിന്റ്, നെയിൽ പോളിഷ് എന്നിവയിൽ ലായനിയായി ഉപയോഗിക്കുന്നു.
മീഥൈൽ അസറ്റേറ്റ് കാർബോണിലേഷന് വ്ധേയമാക്കി അസറ്റിക് അൺഹൈഡ്രൈഡ് നിർമ്മിക്കുന്നു. മോൺസാന്റോ പ്രക്രിയയുടെ മാർഗ്ഗമാണ് ഇവിടെ പ്രയോജനപ്പെടുത്തുന്നത്. [7]
ഇതും കാണുക
[തിരുത്തുക]അവലംബം
[തിരുത്തുക]- ↑ Merck Index, 12th Edition, 6089.
- ↑ 2.0 2.1 2.2 2.3 2.4 2.5 2.6 "NIOSH Pocket Guide to Chemical Hazards #0391". National Institute for Occupational Safety and Health (NIOSH).
- ↑ 3.0 3.1 "Methyl acetate". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ↑ Zeno, W. Wicks, JR, Frank N. Jones, S. Peter Pappas, and Douglas A. Wicks (2007). Organic Coatings. Hoboken, New Jersey: Wiley. ISBN 978-0-471-69806-7.
{{cite book}}: CS1 maint: multiple names: authors list (link) - ↑ "Update: U.S. EPA Exempt Volatile Organic Compounds". American Coatings Association (in അമേരിക്കൻ ഇംഗ്ലീഷ്). 2018-01-30. Archived from the original on 2021-02-08. Retrieved 2019-03-20.
- ↑ Hosea Cheung, Robin S. Tanke, G. Paul Torrence “Acetic Acid” in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. doi:10.1002/14356007.a01_045
- ↑ Zoeller, J. R.; Agreda, V. H.; Cook, S. L.; Lafferty, N. L.; Polichnowski, S. W.; Pond, D. M. (1992). "Eastman Chemical Company Acetic Anhydride Process". Catalysis Today. 13: 73–91. doi:10.1016/0920-5861(92)80188-S.
