ഹൈഡ്രജൻ സയനൈഡ്
(Hydrogen cyanide എന്ന താളിൽ നിന്നും തിരിച്ചുവിട്ടതു പ്രകാരം)
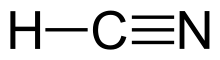
| |||
| |||
| Names | |||
|---|---|---|---|
| IUPAC name | |||
Other names
| |||
| Identifiers | |||
3D model (JSmol)
|
|||
| 3DMet | |||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.747 | ||
| EC Number |
| ||
| KEGG | |||
| MeSH | {{{value}}} | ||
PubChem CID
|
|||
| RTECS number |
| ||
| UNII | |||
| UN number | 1051 | ||
CompTox Dashboard (EPA)
|
|||
| InChI | |||
| SMILES | |||
| Properties | |||
| തന്മാത്രാ വാക്യം | |||
| Molar mass | 0 g mol−1 | ||
| Appearance | Very pale, blue, transparent liquid or colorless gas | ||
| Odor | Oil of bitter almond | ||
| സാന്ദ്രത | 0.687 g mL−1 | ||
| ദ്രവണാങ്കം | |||
| ക്വഥനാങ്കം | |||
| Miscible | |||
| Solubility in ethanol | Miscible | ||
| ബാഷ്പമർദ്ദം | 630 mmHg (20 °C)[3] | ||
Henry's law
constant (kH) |
75 μmol Pa−1 kg−1 | ||
| അമ്ലത്വം (pKa) | 9.21[4] | ||
| Basicity (pKb) | 4.79 | ||
| Refractive index (nD) | 1.2675 [5] | ||
| വിസ്കോസിറ്റി | 201 μPa s | ||
| Structure | |||
| C∞v | |||
| Linear | |||
| 2.98 D | |||
| Thermochemistry | |||
| Std enthalpy of formation ΔfH |
109.9 kJ mol−1 | ||
| Std enthalpy of combustion ΔcH |
-426.5 kJ mol−1 | ||
| Standard molar entropy S |
113.01 J K−1 mol−1 | ||
| Specific heat capacity, C | 71.00 kJ K−1 mol−1 (at 27 °C)[6] | ||
| Hazards | |||
| EU classification | {{{value}}} | ||
| R-phrases | R12, R26/27/28, R50/53 | ||
| S-phrases | (S1/2), S16, S36/37, S38, S45, S53, S59, S61 | ||
| Flash point | {{{value}}} | ||
| Explosive limits | 5.6% - 40.0%[3] | ||
| Lethal dose or concentration (LD, LC): | |||
LC50 (median concentration)
|
501 ppm (rat, 5 min) 323 ppm (mouse, 5 min) 275 ppm (rat, 15 min) 170 ppm (rat, 30 min) 160 ppm (rat, 30 min) 323 ppm (rat, 5 min)[7] | ||
LCLo (lowest published)
|
200 ppm (mammal, 5 min) 36 ppm (mammal, 2 hr) 107 ppm (human, 10 min) 759 ppm (rabbit, 1 min) 759 ppm (cat, 1 min) 357 ppm (human, 2 min) 179 ppm (human, 1 hr)[7] | ||
| NIOSH (US health exposure limits): | |||
PEL (Permissible)
|
TWA 10 ppm (11 mg/m3) [skin][3] | ||
REL (Recommended)
|
ST 4.7 ppm (5 mg/m3) [skin][3] | ||
IDLH (Immediate danger)
|
50 ppm[3] | ||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |||
HCN എന്ന് രാസനാമമുള്ള ഒരു ജൈവ സംയുക്തമാണ്[8] ഹൈഡ്രജൻ സയനൈഡ് (Hydrogen cyanide). നിറമില്ലാത്ത ഈ സംയുക്തം അന്തരീക്ഷ താപനിലയേക്കാൾ അൽപ്പം ഉയർന്ന താപത്തിൽ വാതകമായി മാറുന്നു. തിളനില 25.6 °C (78.1 °F) ആയ ഹൈഡ്രജൻ സയനൈഡ് മാരകമായ വിഷമുള്ള ഒരു പദാർത്ഥമാണ്. വലിയ വിലപിടിച്ച വ്യാവസായിക ഉൽപ്പന്നമായ ഹൈഡ്രജൻ സയനൈഡ് പോളിമറുകളുടെ മുതൽ ഔഷധങ്ങളുടെ വരെ നിർമ്മാണത്തിന് ഉപയോഗിക്കുന്നു.
അവലംബം[തിരുത്തുക]
- ↑ "Hydrogen Cyanide - Compound Summary". PubChem Compound. USA: National Center for Biotechnology Information. 16 September 2004. Identification. Retrieved 2012-06-04.
- ↑ "hydrogen cyanide (CHEBI:18407)". Chemical Entities of Biological Interest. UK: European Bioinformatics Institute. 18 October 2009. Main. Retrieved 2012-06-04.
- ↑ 3.0 3.1 3.2 3.3 3.4 "NIOSH Pocket Guide to Chemical Hazards #0333". National Institute for Occupational Safety and Health (NIOSH).
- ↑ Perrin, D. D. (1982). Ionisation Constants of Inorganic Acids and Bases in Aqueous Solution (2nd ed.). Oxford: Pergamon Press.
- ↑ Patnaik, P. (2002). Handbook of Inorganic Chemicals. McGraw-Hill. ISBN 0-07-049439-8.
- ↑ NIST Chemistry WebBook
- ↑ 7.0 7.1 "Hydrogen cyanide". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ↑ Gail, E.; Gos, S.; Kulzer, R.; Lorösch, J.; Rubo, A.; Sauer, M. (2005), "Cyano Compounds, Inorganic", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a08_159.pub2
{{citation}}: Cite has empty unknown parameter:|authors=(help)CS1 maint: multiple names: authors list (link)
പുറത്തേക്കുള്ള കണ്ണികൾ[തിരുത്തുക]
Hydrogen cyanide എന്ന വിഷയവുമായി ബന്ധപ്പെട്ട ചിത്രങ്ങൾ വിക്കിമീഡിയ കോമൺസിലുണ്ട്.
വർഗ്ഗങ്ങൾ:
- Articles without InChI source
- Articles with changed EBI identifier
- Articles with changed ChemSpider identifier
- ECHA InfoCard ID from Wikidata
- Articles with changed KEGG identifier
- Chembox having DSD data
- വിഷങ്ങൾ
- ഹൈഡ്രജൻ സംയുക്തങ്ങൾ
- ഫ്യൂമിജന്റുകൾ
- സയനൈഡുകൾ
- രക്തത്തിലൂടെ ബാധിക്കുന്ന വിഷങ്ങൾ
- അകാർബണിക സംയുക്തങ്ങൾ
- സയനൈഡ് സംയുക്തങ്ങൾ


