ഗാലിയം ട്രൈക്ലോറൈഡ്
| |

| |
| Names | |
|---|---|
| Other names
Gallium(III) chloride, Trichlorogallium, Trichlorogallane
| |
| Identifiers | |
3D model (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.033.268 |
PubChem CID
|
|
| RTECS number |
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| InChI | |
| SMILES | |
| Properties | |
| തന്മാത്രാ വാക്യം | |
| Molar mass | 0 g mol−1 |
| Appearance | colorless crystals deliquescent |
| സാന്ദ്രത | 2.47 g/cm3 2.053 g/cm3 at melting point |
| ദ്രവണാങ്കം | |
| ക്വഥനാങ്കം | |
| very soluble | |
| Solubility | soluble in benzene, CCl4, CS2 |
| −63.0·10−6 cm3/mol | |
| Hazards | |
| Flash point | {{{value}}} |
| Lethal dose or concentration (LD, LC): | |
LD50 (median dose)
|
4700 mg/kg (rat, oral) |
| Related compounds | |
| Other anions | Gallium(III) fluoride Gallium(III) bromide Gallium(III) iodide |
| Other cations | Aluminium chloride Indium(III) chloride Thallium(III) chloride |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
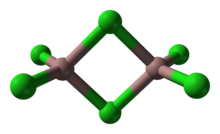
GaCl3 എന്ന രാസസൂത്രമുള്ള സംയുക്തമാണ് ഗാലിയം ട്രൈക്ലോറൈഡ്. Ga2Cl6 എന്ന സമവാക്യത്തോടുകൂടിയ സോളിഡ് ഗാലിയം ട്രൈക്ലോറൈഡ് ഒരു ഡൈമറായി നിലനിൽക്കുന്നുണ്ട്. [1] ഇത് നിറമില്ലാത്തതും എല്ലാ ലായകങ്ങളിലും, ആൽക്കെയ്നുകളിൽ പോലും ലയിക്കുന്നതുമാണ്. ഒരു ലോഹ ഹാലൈഡിനെ സംബന്ധിച്ച് ഇത് അസാധാരണമാണ്. ഗാലിയത്തിന്റെ മിക്ക ഡെറിവേറ്റീവുകളും ഓർഗാനിക് സിന്തസിസിലെ ഒരു റിയാക്ടന്റാണ്. [2]
ലൂയിസ് ആസിഡ് എന്ന നിലയിൽ GaCl3 അലുമിനിയം ട്രൈക്ലോറൈഡിനേക്കാൾ മൃദുവാണ്.
തയ്യാറാക്കൽ
[തിരുത്തുക]മൂലകങ്ങളിൽ നിന്ന് ഗാലിയം ട്രൈക്ലോറൈഡ് തയ്യാറാക്കാം, ക്ലോറിൻ പ്രവാഹത്തിൽ ഗാലിയം ലോഹം ചൂടാക്കുന്നു, സബ്ലിമേഷൻ വഴി ഉൽപ്പന്നത്തെ ശുദ്ധീകരിക്കാം. [3] [4]
- 2 Ga + 3 Cl2 → 2 GaCl3
ഗാലിയം ഓക്സൈഡ് തയോനൈൽ ക്ലോറൈഡ് ഉപയോഗിച്ച് ചൂടാക്കിയും ഇത് തയ്യാറാക്കാം: [5]
- Ga2O3 + 3 SOCl2 → 2 GaCl3 + 3 SO2
ഗാലിയം ലോഹം ഹൈഡ്രോക്ലോറിക് ആസിഡുമായി സാവധാനം പ്രതികരിക്കുന്നു. ഈ പ്രതികരണത്തിന്റെ ഫലമായി സാവധാനത്തിൽ ഹൈഡ്രജൻ വാതകം ഉണ്ടാവുന്നു.
ഘടന
[തിരുത്തുക]ഒരു സോളിഡ് എന്ന നിലയിൽ, ഇത് രണ്ട് ബ്രിഡ്ജിംഗ് ക്ലോറൈഡുകളുള്ള ഒരു ബിടെട്രാഹൈഡ്രൽ ഘടന സ്വീകരിക്കുന്നു. ഇതിന്റെ ഘടന അലുമിനിയം ട്രൈബ്രോമൈഡിനോട് സാമ്യമുള്ളതാണ്. അതിന്റെ തന്മാത്രാ സ്വഭാവത്തിന്റെയും അനുബന്ധ താഴ്ന്ന ലാറ്റിസ് ഊർജ്ജത്തിന്റെയും അനന്തരഫലമായി, ഗാലിയം ട്രൈക്ലോറൈഡിന് അലുമിനിയം, ഇൻഡിയം ട്രൈഹാലൈഡുകൾ എന്നിവയേക്കാൾ ദ്രവണാങ്കം കുറവാണ്. Ga2Cl6 ന്റെ സമവാക്യം പലപ്പോഴും Ga2(μ-Cl)2Cl4 എന്നാണ് എഴുതുന്നത്. വാതകാവസ്ഥയിൽ, ഡൈമറുകൾ ത്രികോണ പ്ലാനർ മോണോമറുകളായി വേർതിരിയുന്നു.
ഉപയോഗങ്ങൾ
[തിരുത്തുക]ഓർഗാനിക് സിന്തസിസ്
[തിരുത്തുക]ഫ്രീഡെൽ-ക്രാഫ്റ്റ്സ് പ്രതിപ്രവർത്തനത്തിൽ ഉപയോഗിക്കുന്നപോലുള്ള ഒരു ലൂയിസ് ആസിഡ് ഉൽപ്രേരകമാണ് ഗാലിയം ട്രൈക്ലോറൈഡ്. കാർബൺ-കാർബൺ ട്രിപ്പിൾ ബോണ്ടുള്ള സംയുക്തങ്ങളുടെ കാർബോഗലേഷൻ പ്രതിപ്രവർത്തനങ്ങളിലും ഇത് ഉപയോഗിക്കുന്നു. ഓർഗാനോഗാലിയം റിയേജന്റുകളുടെ ഒരു മുന്നോടിയാണിത്. പല ജൈവ പ്രതിപ്രവർത്തനങ്ങളിലും ഇത് ഒരു ഉത്തേജകമായി ഉപയോഗിക്കുന്നു. [2]
അവലംബം
[തിരുത്തുക]- "Gallium". WebElements Periodic Table.
- ↑ Wells, A.F. (1984) Structural Inorganic Chemistry, Oxford: Clarendon Press. ISBN 0-19-855370-6.
- ↑ 2.0 2.1 Yamaguchi, Masahiko; Matsunaga, Shigeki; Shibasaki, Masakatsu; Michelet, Bastien; Bour, Christophe; Gandon, Vincent (2014), "Gallium Trichloride", Encyclopedia of Reagents for Organic Synthesis, John Wiley & Sons, Ltd, pp. 1–8, doi:10.1002/047084289x.rn00118u.pub3, ISBN 9780470842898
- ↑ S.C. Wallwork I.J.Worral J.Chem. Soc 1965,1816
- ↑ Kovar, R. A. "Gallium Trichloride" Inorganic Syntheses, 1977, volume XVII, pp 167-172. ISBN 0-07-044327-0
- ↑ H.Hecht, G.Jander, H.Schlapmann Z. Anorg. Allgem. Chem. Vol.254, p.255 (1947)
പുറംകണ്ണികൾ
[തിരുത്തുക]- "Emergency First Aid Treatment Guide - Gallium Trichloride". United States Environmental Protection Agency. Archived from the original on 2004-11-12.
