ബോർ മാതൃക
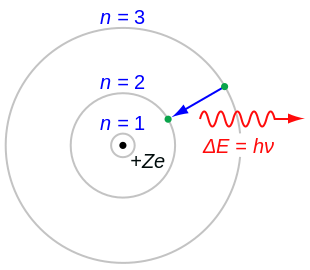
നീൽസ് ബോർ നിർദ്ദേശിച്ച ആറ്റത്തിന്റെ മാതൃകയാണ് ബോർ മാതൃക എന്നറിയപ്പെടുന്നത്. ഈ മാതൃക പ്രകാരം ആറ്റം എന്നത് പോസിറ്റിവ് ചാർജ്ജുള്ള ഒരു ന്യൂക്ലിയസും അതിനെ വൃത്താകാരമായ ഭ്രമണപഥത്തിൽ വലം വയ്ക്കുന്ന ഇലക്ട്രോണുകളും ചേർന്നതാണ്. സൗരയൂഥത്തിൽ ഗ്രഹങ്ങൾ സൂര്യനു ചുറ്റും വല വയ്ക്കുന്നതിനു സമാനമാണ് ഇത്. ഗുരുത്വാകർഷണബലത്തിനു പകരം സ്ഥിത വൈദ്യുത ബലങ്ങളാണ് കണങ്ങൾ തമ്മിലുള്ള ആകർഷണത്തിന് ഹേതുവാകുന്നത് എന്നു മാത്രം. ഇത് മുൻപുണ്ടായിരുന്ന ക്യുബിക് മോഡൽ(1902), പ്ലം പുഡിങ് മാതൃക(1904), സാറ്റേണിയൻ മോഡൽ(1904), റൂഥർഫോർഡ് മോഡൽ(1911) എന്നിവയിൽ നിന്നും ഉരുത്തിരിഞ്ഞു വന്നതായിരുന്നു. ബോർ മാതൃക, റൂഥർഫോർഡ് മാതൃകയുടെ, ക്വാണ്ടം ഭൗതികശാസ്ത്രത്തിൽ അധിഷ്ഠിതമായ രൂപമായതിനാൽ പലപ്പോഴും ഇത് റൂഥർഫോർഡ്-ബോർ മാതൃക എന്ന പേരിലും അറിയപ്പെടുന്നു.
