അമീനുകൾ
| പ്രൈമറി അമീൻ | സെക്കൻഡറി അമീൻ | ടെർടിയറി അമീൻ |
|---|---|---|
 |
 |
 |
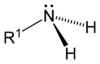
അമോണിയയിലെ ഹൈഡ്രജനെ ആൽക്കൈൽ ഗ്രൂപ്പോ അരൈൽ ഗ്രൂപ്പോ കൊണ്ടു പ്രതിസ്ഥാപിച്ചു കിട്ടുന്ന വ്യുത്പന്നങ്ങളാണ് അമീനുകൾ. മീഥൈൽ അമീൻ (CH3 NH2), ഈഥൈൽ അമീൻ (C2H5 NH2), ഫിനൈൽ അമീൻ (C6H5 NH2) അഥവാ അനിലിൻ എന്നിവ ഉദാഹരണങ്ങൾ. അമോണിയയിലെ ഒരു ഹൈഡ്രജനെമാത്രം ആദേശിച്ചുകിട്ടുന്ന അമീനുകളെ പ്രൈമറി എന്നും രണ്ടു ഹൈഡ്രജൻ അണുക്കളെ ആദേശിച്ചു കിട്ടുന്നവയെ സെക്കൻഡറി [ഉദാ. (CH3)2NH] എന്നും, മൂന്നു ഹൈഡ്രജൻ അണുക്കളെ ആദേശിച്ചു കിട്ടുന്നവയെ ടെർഷ്യറി [ഉദാ. (CH3)3N] എന്നും വിശേഷിപ്പിക്കാറുണ്ട്. സെക്കൻഡറി അമീനുകളിലും ടെർഷ്യറി അമീനുകളിലും പ്രതിസ്ഥാപകഗ്രൂപ്പുകൾ (substituent groups) ഒരേ വിധത്തിലാണെങ്കിൽ അവയെ സരള(simple) അമീനുകൾ എന്നു പറഞ്ഞുവരുന്നു. മുകളിൽ കൊടുത്തവതന്നെയാണ് ഇതിന് ഉദാഹരണങ്ങൾ. എന്നാൽ പ്രതിസ്ഥാപകഗ്രൂപ്പുകൾ ഭിന്നങ്ങളാണെങ്കിൽ അവ മിശ്ര (mixed) അമീനുകളാണ്. മീഥൈൽ ഈഥൈൽ അമീൻ (CH3.C2H5.NH), മീഥൈൽ ഫിനൈൽ അമീൻ (CH3.C6H5.NH), മീഥൈൽ ഈഥൈൽ ഫിനൈൽ അമീൻ (CH3.C2H5.C6H5.N) മുതലായവ ദൃഷ്ടാന്തങ്ങൾ. അമീനുകളിൽ കാർബണിക ഗ്രൂപ്പുകൾ നൈട്രജനുമായി നേരിട്ടാണു ബന്ധപ്പെട്ടിരിക്കുന്നത്. അങ്ങനെ ഘടിതങ്ങളായ ഗ്രൂപ്പുകൾ മുഴുവനും ആലിഫാറ്റികങ്ങൾ (aliphatic) ആണെങ്കിൽ അവ ആലിഫാറ്റിക് അമീനുകളാണ്; ഏതെങ്കിലും ഒന്ന് ആരൊമാറ്റികം (aromatic) ആണെങ്കിൽ അവ ആരൊമാറ്റിക് അമീനുകളാണ്. ഗ്രൂപ്പുകളിൽ ഒന്നെങ്കിലും അപൂരിതം (unsaturated) ആണെങ്കിൽ അവ അപൂരിത അമീനുകളെന്നു പറയപ്പെടുന്നു (ഉദാ. വിനൈൽ അമീൻ, (CH2=CH.NH2). ഒരു തന്മാത്രയിൽ ഒന്നിലധികം അമിനൊ ഗ്രൂപ്പുകൾ ഉണ്ടെങ്കിൽ സംഖ്യാനുസരണം അവയെ ഡൈ അമീനുകൾ, ട്രൈ അമീനുകൾ എന്നു വിളിക്കുന്നു. അമീനുകൾക്ക് പൊതുവേ ചില സവിശേഷതകൾ ഉണ്ടെങ്കിലും ഓരോ വർഗത്തിൽ പെട്ടവയേയും പ്രത്യേകമെടുത്തു പഠനം നടത്തുകയാണ് പതിവ്.
ആലിഫാറ്റിക അമീനുകൾ[തിരുത്തുക]
ഏതാനും ആലിഫാറ്റിക അമീനുകൾ ചില ചെടികളിലും മറ്റും കണ്ടു വരുന്നുണ്ടെങ്കിലും കൃത്രിമ മാർഗങ്ങളിലൂടെയാണ് ഇവ സാധാരണമായി ലഭ്യമാക്കി വരുന്നത്. ഒരു ആൽക്കൈൽ ഹാലൈഡും ആൽക്കഹോളിൽ ലയിപ്പിച്ച അമോണിയയും കൂട്ടിച്ചേർത്ത് അടച്ച ഒരു പാത്രത്തിൽവച്ചു ചൂടാക്കിയാൽ പ്രൈമറി, സെക്കൻഡറി, ടെർഷ്യറി അമീനുകളുടെ ഒരു മിശ്രിതം ലഭിക്കുന്നു. അല്പം ക്വാർട്ടേർണറി (quarternary) അമോണിയം ലവണവും ഉണ്ടായേക്കാം. ഇതു ഹോഫ്മാൻ എന്ന ശാസ്ത്രജ്ഞൻ കണ്ടുപിടിച്ച സംശ്ളേഷണ പ്രക്രിയയാണ്.
- R.X+NH3 -------->R.NH2+HX
- R.NH2+R.X -------->R2.NH+HX
- R2.NH+R.X -------->R3.N+HX
- R3.N+R.X --------->R4N+X -
ഈ സമവാക്യങ്ങളിൽ R എന്നത് ഒരു ആൽ ക്കൈൽ ഗ്രൂപ്പിനെയും ഉദാ. [( CH3;C2H5)] X എന്നത് ഒരു ഹാലൈഡ് ഗ്രൂപ്പിനെയും (ഉദാ. ക്ലോറൈഡ്; ബ്രോമൈഡ്) പ്രതിനിധാനം ചെയ്യുന്നു. നാലാമത്തെ സമവാക്യത്തിൽ ഉത്പന്നമായി ലഭിക്കുന്നത് ഒരു ക്വാർട്ടേർണറി അമോണിയം ലവണമാണ്. ഉത്പന്നങ്ങളുടെ മിശ്രിതത്തിൽ നിന്ന് ഘടകങ്ങളെ വേർതിരിച്ചെടുക്കുന്നതിന് മാർഗങ്ങളുണ്ട്.
പ്രൈമറി അമീനുകളെ ഉത്പാദിപ്പിക്കുന്നതിന് പ്രത്യേകമായ ചില വിധികളും ഇല്ലാതില്ല. ഒരു അമ്ള അമൈഡും (acid amide) ബ്രോമിനും സോഡിയം ഹൈഡ്രോക്സൈഡും ചേർത്തു ചൂടാക്കുമ്പോൾ പ്രൈമറി അമീൻ ലഭിക്കുന്നു.
- R.CO.NH2+Br24NaOH------->R.NH2+2NaBr+Na2CO3+2H2O
ഒരു നൈട്രൊ യൌഗികം നിരോക്സീകരിച്ച് മിക്കവാറും ശുദ്ധമായ പ്രൈമറി അമീൻ ലഭിക്കുന്നു.
- R.NO2+6H------Sn+HCI------>R.NH22H2O
പ്രൈമറി അമീനുകൾ നിർമ്മിക്കുവാൻ ഗബ്രിയൽ എന്ന ശാസ്ത്രജ്ഞൻ കണ്ടുപിടിച്ച ഒരു രീതിയും പ്രാധാന്യമുള്ളതാണ്.
സെക്കൻഡറി അമീനുകൾ, ടെർഷ്യറി അമീനുകൾ, ക്വാർട്ടേർണറി ലവണങ്ങൾ എന്നിവയുടെ നിർമ്മാണത്തിനും അനുയോജ്യമാർഗങ്ങൾ ആവിഷ്കരിക്കപ്പെട്ടിട്ടുണ്ട്.
ഗുണധർമങ്ങൾ[തിരുത്തുക]
താഴ്ന്ന അമീനുകൾ അമോണിയയുടെ ഗന്ധമുള്ള വാതകങ്ങളാണ്. ഉയർന്ന അമീനുകൾ ദ്രവങ്ങളോ ഖരങ്ങളോ ആയിരിക്കും. ഗന്ധം പൊതുവേ അരോചകമായിരിക്കും. എല്ലാം വായുവിൽ കത്തിക്കപ്പെടാവുന്നവയാണ്. അമോണിയയേക്കാൾ ബേസികത കൂടിയവയാണ്. ആൽക്കൈൽ ഗ്രൂപ്പുകളുടെ എണ്ണം കൂടുന്തോറും ബേസികത കൂടുന്നു. ക്വാർട്ടേർണറി അമോണിയം ഹൈഡ്രോക്സൈഡ് ശക്തിയേറിയ കാർബണിക ബേസുകൾക്കു തുല്യമാണ്. എല്ലാ അമീനുകളും അമ്ലങ്ങളോടു ചേർന്നു ലവണങ്ങളുണ്ടാക്കുന്നു.
RNH2 + HCI --------> R NH2 HCI
പ്ലാറ്റിനം ക്ലോറൈഡ് ലായനി ചേർത്താൽ മിക്കവാറും എല്ലാ അമീനുകളിലും നിന്നു ലേയത്വം കുറഞ്ഞ ക്ലോറൊ പ്ലാറ്റിനേറ്റ് ലവണങ്ങൾ ഉണ്ടാകും. പ്രൈമറി അമീനുകളും സെക്കൻഡറി അമീനുകളും അസറ്റൈൽ ക്ലോറൈഡ് (R.COCl) അസറ്റിക് അൻഹൈഡ്രൈഡ് (R CO.O CO.R) എന്നിവയുമായി പ്രവർത്തിച്ച് ബേസികത കുറഞ്ഞ അസറ്റൈൽ വ്യുത്പന്നങ്ങൾ ലഭ്യമാക്കുന്നു. പ്രൈമറി അമീനുകൾ നൈട്രസ് അമ്ലവുമായി പ്രവർത്തിച്ച് ആൽക്കഹോളുകൾ നല്കുന്നു. ഇതേ സാഹചര്യത്തിൽ സെക്കൻഡറി അമീനുകൾ ലേയത്വം കുറഞ്ഞതും മിക്കവാറും തൈലരൂപത്തിലുള്ളതുമായ നൈട്രോസമീനുകൾ (nitrosamines) ആണ് തരുന്നത്. ടെർഷ്യറി അമീനുകൾ ആൽഡിഹൈഡുകളുമായിച്ചേർന്ന് ഷിഫ്-ബേസുകൾ (schiff's base) ഉണ്ടാക്കുന്നു.
R.NH2 + O CHR --------> R.N = HC R + H2O
ഒരു പ്രൈമറി അമീനിൽ ക്ലോറോഫോം, ആൽക്കഹോളിക പൊട്ടാഷ് എന്നിവ ചേർത്തു ചൂടാക്കുമ്പോൾ അസഹ്യദുർഗന്ധമുള്ള ഐസൊ സയനൈഡുകൾ (കാർബിലമീനുകൾ) ഉണ്ടാകുന്നതാണ്. 'ഹോഫ്മൻ കാർബിലമീൻ അഭിക്രിയ' എന്ന് ഇതിനെ വിളിക്കുന്നു. മറ്റു വിഭാഗത്തിൽപെട്ട അമീനുകൾ ഇപ്രകാരം പ്രവർത്തിക്കാത്തതിനാൽ പ്രൈമറി അമീനുകൾക്ക് ഇത് ഒരു നിർണായകപരീക്ഷണമാണ്. ടെർഷ്യറി അമീനുകൾ പെർ ആസിഡുകളുമായി പ്രവർത്തിച്ച് അമീൻ ഓക്സൈഡുകൾ ലഭ്യമാക്കുന്നു. ക്വാർട്ടേർണറി ലവണങ്ങൾ ചൂടാക്കിയാൽ വിഘടിച്ച് മിക്കവാറും ഒലിഫീനുകൾ (olefins) ഉണ്ടാക്കുന്നു.
ആരൊമാറ്റിക അമീനുകൾ[തിരുത്തുക]
ഇവയിൽ പ്രൈമറി ആരൊമാറ്റിക അമീനുകൾക്കാണ് പ്രാധാന്യം. സാമാന്യ ഫോർമുല, Ar.NH2 (Ar=ഏതെങ്കിലും ഒരു ആരൊമാറ്റിക ഗ്രൂപ്പ്). ആരൊമാറ്റിക ഹൈഡ്രൊ കാർബണുകളിൽ നിന്ന് ആരംഭിക്കുന്നതായാൽ നൈട്രേഷൻവഴി ലഭിച്ച നൈട്രൊ യൗഗികത്തെ അപചയിച്ച് ആരൊമാറ്റിക അമീനുകൾ ലഭ്യമാക്കാം. ഉദാഹരണമായി ബെൻസീനിൽനിന്ന് അനിലീൻ. ഈ അപചയത്തിന് ഉപയോഗിക്കുന്നത് ഹൈഡ്രൊക്ലോറിക് അമ്ളവും ടിൻ അല്ലെങ്കിൽ ഇരുമ്പും ചേർന്ന മിശ്രിതവുമാണ്. പ്ളാറ്റിനം, പലേഡിയം, നിക്കൽ എന്നിവയിൽ ഏതെങ്കിലുമൊരു ലോഹം ഉത്പ്രേരകമായിട്ടുപയോഗിച്ചാൽ ഹൈഡ്രജൻകൊണ്ടു നേരിട്ടുതന്നെ നൈട്രൊ യൗഗികങ്ങളെ അമീൻ ആക്കി മാറ്റാം. സംഗതങ്ങളായ (corresponding) നൈട്രോസൊ, അസൊ (nitroso;azo) എന്നീ വിഭാഗത്തിൽപെട്ട യൗഗികങ്ങളെ അപചയിച്ചും ആരൊമാറ്റിക അമീനുകൾ ലഭ്യമാക്കാം. ആലിഫാറ്റിക അമീനുകളുടെ കാര്യത്തിൽ നിർദ്ദേശിക്കപ്പെട്ട പൊതുമാർഗങ്ങളും സ്വീകാര്യങ്ങളാണ്. ക്ലോറോ ബെൻസീൻ (C6H5Cl) അമോണിയയുമായി പ്രവർത്തിക്കണമെങ്കിൽ ഉയർന്ന ഊഷ്മാവും ഉത്പ്രേരകസഹായവും ആവശ്യമാണ്.
ഗുണധർമങ്ങൾ[തിരുത്തുക]
ആരൊമാറ്റിക അമീനുകൾ പൊതുവേ വർണരഹിതങ്ങളായ ദ്രവങ്ങളോ ഖരങ്ങളോ ആയിരിക്കും. പക്ഷേ, അല്പകാലവായുസമ്പർക്കത്താൽ അവയ്ക്ക് കറുപ്പുനിറം ഉണ്ടാകും. ഓക്സീകരണം വഴി കറുത്തനിറത്തിലുള്ള പുതിയ പദാർഥങ്ങൾ ഉണ്ടാകുന്നു എന്നതാണ് അതിനു കാരണം. ആലിഫാറ്റിക അമീനുകളുടേതുപോലെ രൂക്ഷഗന്ധമില്ല. ജലത്തിൽ ലേയത്വം കുറവാണ്. നേർത്ത ഹൈഡ്രൊക്ളോറിക് അമ്ലത്തിലും കാർബണിക ലായകങ്ങളിലും അലിയും. ബേസികത അലിഫാറ്റിക അമീനുകളുടേതിനെക്കാൾ കുറവാണ്. ആരൊമാറ്റികഗ്രൂപ്പുകളുടെ എണ്ണം കൂടുന്തോറും ബേസികത ചുരുങ്ങുന്നു. ട്രൈഫിനൈൽ അമീൻ ബേസികത തീരെ ഇല്ലാത്ത ഒരു വസ്തുവാണ്. ആരൊമാറ്റിക അമീനുകൾക്ക് സാമാന്യേന വിഷാലുത്വം ഉണ്ട്.
ആരൊമാറ്റിക അമീനുകളെ ഹൈഡ്രൊക്ളോറിക് അമ്ളത്തിൽ ലയിപ്പിച്ചശേഷം തണുപ്പിച്ച് സോഡിയം നൈട്രേറ്റ് ചേർക്കുമ്പോൾ ഡൈഅസോണിയം ലവണങ്ങൾ (diazonium salts) ഉണ്ടാകുന്നു. ആലിഫാറ്റിക അമീനുകൾക്ക് ഈ ഗുണമില്ല.
പാർശ്വശൃംഖലാപ്രതിസ്ഥാപിത അമീനുകൾ[തിരുത്തുക]
ഒരു ആരൊമാറ്റിക ന്യൂക്ളിയസ്സിനോട് നേരിട്ടു ബന്ധപ്പെടാതെ ഒന്നോ അതിലധികമോ കാർബൺ-അണുക്കൾക്കപ്പുറം ബേസിക് നൈട്രജൻ സ്ഥിതിചെയ്യുമ്പോൾ ഉണ്ടാകുന്ന അമീനുകളാണ് ഇവ. ഉദാ. C6H5CH2NH2 (ഫിനൈൽ മീഥൈൽ അമീൻ); C6H5 CH2. CH2. NH2 (ഫിനൈൽ ഈഥൈൽ അമീൻ) എന്നിവ. ആലിഫാറ്റിക അമീനുകൾക്കു നിർദ്ദേശിച്ച രീതിയനുസരിച്ച് ഇവയെ പരീക്ഷണശാലകളിൽ ലഭ്യമാക്കാം. ഇവയ്ക്ക് ഗുണധർമങ്ങളിലും അവയോടാണ് സാദൃശ്യം.
ഡൈഅമീനുകൾ[തിരുത്തുക]
രണ്ട് അമിനൊ ഗ്രൂപ്പുകളുള്ള അമീനുകളാണ് ഇവ. എഥിലീൻ ഡൈ അമീൻ (NH2.CH2.CH2,NH), ടെട്രാമെഥിലീൻ ഡൈ അമീൻ (NH2.CH2.CH22. CH2.CH2. NH2) എന്നിവ രണ്ടു ഉദാഹരണങ്ങളാണ്. മോണോ അമീനുകൾക്കു നിർദ്ദേശിച്ച രീതികൾക്ക് സദൃശങ്ങളായ രീതികളിലൂടെ ഇവ ലഭ്യമാക്കാം.
| കടപ്പാട്: കേരള സർക്കാർ ഗ്നൂ സ്വതന്ത്ര പ്രസിദ്ധീകരണാനുമതി പ്രകാരം ഓൺലൈനിൽ പ്രസിദ്ധീകരിച്ച മലയാളം സർവ്വവിജ്ഞാനകോശത്തിലെ അമീനുകൾ എന്ന ലേഖനത്തിന്റെ ഉള്ളടക്കം ഈ ലേഖനത്തിൽ ഉപയോഗിക്കുന്നുണ്ട്. വിക്കിപീഡിയയിലേക്ക് പകർത്തിയതിന് ശേഷം പ്രസ്തുത ഉള്ളടക്കത്തിന് സാരമായ മാറ്റങ്ങൾ വന്നിട്ടുണ്ടാകാം. |
