സംവൃതവ്യൂഹം
പുറത്തേയ്ക്കോ അകത്തേയ്ക്കോ ദ്രവ്യത്തെ കടത്തിവിടാത്ത തരം വ്യൂഹങ്ങളാണ് സംവൃതവ്യൂഹം അഥവാ Closed System. ഇത് ഊർജ്ജത്തെ കടത്തിവിടുകയില്ല.
ഭൗതികശാസ്ത്രത്തിൽ[തിരുത്തുക]
ഉദാത്തബലതന്ത്രത്തിൽ[തിരുത്തുക]
ബലതന്ത്രപ്രകാരം സംവൃതവ്യൂഹം എന്നാൽ പ്രാന്തവുമായി (surroundings) ദ്രവ്യത്തെ വിനിമയം ചെയ്യാത്തതും എന്നാൽ യാതൊരു സഞ്ചിത ബാഹ്യബലത്തിന്റെ അധീനതയിലല്ലാത്തതുമായ ഭൗതികവ്യൂഹമാണ്. [1][2] ബലതന്ത്രത്തിലെ സംവൃതവ്യൂഹമെന്നാൽ താപഗതികത്തിലെ thermodynamics ഒരു കവചിതവ്യൂഹം isolated system പോലെതന്നെയാണ്. ഒരു പ്രത്യേക പ്രശ്നനിർദ്ധാരണമോ പരീക്ഷണമോ ചെയ്യുന്ന സമയത്ത് അതിന്റെ ഫലത്തെ ബാധിച്ചേയ്ക്കാവുന്ന ഘടകങ്ങളെ പരിമിതപ്പെടുത്തുന്നതിനാണ് സംവൃതവ്യൂഹം ഉപയോഗിക്കുന്നത്.
താപഗതികത്തിൽ[തിരുത്തുക]
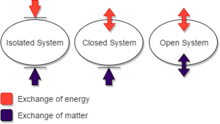
താപഗതികത്തിൽ ഒരു സംവൃതവ്യൂഹം എന്നാൽ ദ്രവ്യത്തെ വിനിമയം ചെയ്യാത്തതും എന്നാൽ ഊർജ്ജത്തെ യാന്ത്രികപ്രവൃത്തിയായോ താപമായോ വിനിമയം ചെയ്യുന്നതുമായ വ്യൂഹമാണ്. ഒരു കവചിതവ്യൂഹം ഊർജ്ജമോ ദ്രവ്യമോ പ്രാന്തവുമായി വിനിമയം ചെയ്യുന്നില്ല. അതേസമയം വിവൃതവ്യൂഹമാകട്ടെ ദ്രവ്യത്തെയും ഊർജ്ജത്തെയും കടത്തിവിടുന്നു. [3][4][5][6][7][8][9]
ഒരേ ഇനം ആറ്റങ്ങളോ തന്മാത്രകളോ മാത്രമുളള ഒരു ലഘുവ്യൂഹത്തിന് സുനിശ്ചിത എണ്ണം ദ്രവ്യകണികകളേ ഉണ്ടാകുകയുളളു. എന്നാൽ, രാസപ്രവർത്തനത്തിന് വിധേയമാകുന്ന വ്യൂഹങ്ങളിൽ വിവിധ തരം തന്മാത്രകൾ ഉണ്ടാക്കപ്പെടുകയും നശിപ്പിക്കപ്പെടുകയും ചെയ്യും. ഇത്തരം സന്ദർഭങ്ങളിൽ മൗലിക ആറ്റങ്ങളുടെ ആകെ എണ്ണം അതേപടി നിലനിർത്തപ്പെട്ടു എന്നതിന്റെ അടിസ്ഥാനത്തിലാണ് ആ വ്യൂഹം സംവൃതവ്യൂഹം എന്ന് പറയപ്പെടുന്നത്. ഗണിതപരമായി:
ഇതിൽ എന്നാൽ ജെ-തരം (j-type) തന്മാത്രകളുടെ എണ്ണം, എന്നാൽ j തന്മാത്രയിലെ i എന്ന മൂലകത്തിന്റെ ആറ്റങ്ങളുടെ എണ്ണവും bi എന്നാൽ i എന്ന മൂലകത്തിന്റെ ആകെ ആറ്റങ്ങളുടെ എണ്ണവും ആണ്. വ്യൂഹം സംവൃതമായതിനാൽ ഇവ അചരമായി നിലനിൽക്കും. വ്യൂഹത്തിലെ ഓരോ മൂലകത്തിനും ഇതുപോലുളള ഓരോ സൂത്രവാക്യം ഉണ്ടായിരിക്കും.
സങ്കീർണമായ താപഗതികപ്രശ്നങ്ങൾ നിർദ്ധാരണം ചെയ്യുമ്പോൾ സംവൃതവ്യൂഹത്തിന് വളരെ പ്രാധാന്യമുണ്ട്. സംവൃതവ്യൂഹം ഉപയോഗിക്കുകവഴി പ്രശ്നത്തിന്റെയോ പരീക്ഷണത്തിന്റെയോ ഫലങ്ങളെ സ്വാധീനിക്കാവുന്ന ബാഹ്യഘടകങ്ങളെ ഒഴിവാക്കി ഫലനിർണയം അനായാസമാക്കുന്നതിന് സം സഹായകമാകും. താപസന്തുലനത്തിലൂടെ സന്ദർഭത്തെ ലഘൂകരിക്കേണ്ടി വരുന്ന സന്ദർഭങ്ങളിലും സംവൃതവ്യൂഹം ഉപയോഗപ്രദമാണ്.
രസതന്ത്രത്തിൽ[തിരുത്തുക]
രസതന്ത്രത്തിൽ ഒരു സംവൃതവ്യൂഹം എന്നാൽ അഭികാരകങ്ങളും ഉത്പന്നങ്ങളും വ്യൂഹത്തിൽ നിന്നും രക്ഷപ്പെടാതെ താപത്തെ മാത്രം സ്വതന്ത്രമായി പുറത്തുപോകാനനുവദിക്കുന്ന വ്യൂഹമാണ്. താപസന്തുലനം ആവശ്യമായ പരീക്ഷണങ്ങൾ നടത്തുമ്പോഴാണ് സംവൃതവ്യൂഹം ഉപോയോഗിക്കുന്നത്.
ഇവയും കാണുക[തിരുത്തുക]
- വ്യൂഹസിദ്ധാന്തം
- ചലനാത്മക വ്യൂഹം (Dynamical system )
- കവചിത വ്യൂഹം
- വിവൃത വ്യൂഹം
- സംവേദനവും പ്രതികരണവും
- താപഗതിക വ്യൂഹങ്ങൾ
അവലംബം[തിരുത്തുക]
- ↑ Rana, N.C.; P.S. Joag (1991). Classical Mechanics. p. 78. ISBN 978-0-07-460315-4.
- ↑ Landau, L.D.; E.M. Lifshitz (1976). Mechanics (third ed.). p. 8. ISBN 978-0-7506-2896-9.
- ↑ Prigogine, I., Defay, R. (1950/1954). Chemical Thermodynamics, Longmans, Green & Co, London, p. 66.
- ↑ Tisza, L. (1966). Generalized Thermodynamics, M.I.T Press, Cambridge MA, pp. 112–113.
- ↑ Guggenheim, E.A. (1949/1967). Thermodynamics. An Advanced Treatment for Chemists and Physicists, (1st edition 1949) 5th edition 1967, North-Holland, Amsterdam, p. 14.
- ↑ Münster, A. (1970). Classical Thermodynamics, translated by E.S. Halberstadt, Wiley–Interscience, London, pp. 6–7.
- ↑ Haase, R. (1971). Survey of Fundamental Laws, chapter 1 of Thermodynamics, pages 1–97 of volume 1, ed. W. Jost, of Physical Chemistry. An Advanced Treatise, ed. H. Eyring, D. Henderson, W. Jost, Academic Press, New York, lcn 73–117081, p. 3.
- ↑ Tschoegl, N.W. (2000). Fundamentals of Equilibrium and Steady-State Thermodynamics, Elsevier, Amsterdam, ISBN 0-444-50426-5, p. 5.
- ↑ Silbey, R.J., Alberty, R.A., Bawendi, M.G. (1955/2005). Physical Chemistry, fourth edition, Wiley, Hoboken NJ, p. 4.



