ഫ്രാങ്ക്-ഹേർട്സ് പരീക്ഷണം
നീൽസ് ബോറിന്റെ ആറ്റം മാതൃകയ്ക്ക് തെളിവ് നൽകിയ ഭൗതികശാസ്ത്രപരീക്ഷണമാണ് ഫ്രാങ്ക്-ഹേർട്സ് പരീക്ഷണം (Franck–Hertz experiment). 1914-ൽ ജർമ്മൻ ഭൗതികശാസ്ത്രജ്ഞരായ ജെയിംസ് ഫ്രാങ്ക്, ഗുസ്താവ് ലുഡ്വിഗ് ഹേർട്സ് എന്നിവർ ചേർന്നാണ് ഈ പരീക്ഷണം നടത്തിയത്. ആറ്റങ്ങൾക്ക് ഊർജ്ജം ചില പ്രത്യേക അളവുകളിൽ (quanta) മാത്രമേ സ്വീകരിക്കാനാവൂ എന്ന് ഈ പരീക്ഷണം തെളിയിച്ചു. അണുകേന്ദ്രത്തിന് ചുറ്റും ഇലക്ട്രോണുകൾ ചില നിശ്ചിത ഊർജ്ജാവസ്ഥകളിൽ മാത്രമേ കാണപ്പെടൂ എന്ന് പരികല്പന നടത്തിയ ബോർ ആറ്റം മാതൃകയ്ക്ക് ഇത് ഉപോദ്ബലകമായി. ഈ പരീക്ഷണത്തിന് ഇരുവർക്കും 1925-ൽ ഭൗതികശാസ്ത്രത്തിനുള്ള നോബൽ സമ്മാനം ലഭിച്ചു[1].
ചരിത്രം[തിരുത്തുക]
1913-ലാണ് നീൽസ് ബോർ തന്റെ ആറ്റം മാതൃക പുറത്തിറക്കിയത്. 1911-ൽ പുറത്തുവന്ന റുഥർഫോർഡ് ആറ്റം മാതൃകയെ അടിസ്ഥാനമാക്കിയായിരുന്നു ഇത്[2]. പ്രവേഗത്തിൽ മാറ്റം വരുന്ന ഇലക്ട്രോൺ, വികിരണം വഴി ഊർജ്ജം നഷ്ടപ്പെട്ട് അണുകേന്ദ്രത്തിനുള്ളിലേക്ക് പതിക്കും എന്ന വിരോധാഭാസത്തിന് ഉത്തരം കാണാൻ റുഥർഫോർഡ് മാതൃകയ്ക്ക് സാധിച്ചിരുന്നില്ല. അണുകേന്ദ്രത്തിനു ചുറ്റും ഭ്രമണം ചെയ്യുന്ന ഇലക്ട്രോണുകൾക്ക് ചില പ്രത്യേക ഭ്രമണപഥങ്ങളിലേ അത് സാധിക്കുകയുള്ളൂ എന്നും ചില നിശ്ചിത വിലകൾ മാത്രമേ ഇലക്ട്രോണിന്റെ ഊർജ്ജം, കോണീയ സംവേഗം എന്നിവയ്ക്ക് ഉണ്ടാകൂ എന്നും ബോർ സിദ്ധാന്തിച്ചു[3]. ഈ ഊർജ്ജാവസ്ഥകളിലെ ഇലക്ട്രോണുകൾ ത്വരണം മൂലമുള്ള വികിരണത്തിലൂടെ ഊർജ്ജം നഷ്ടപ്പെടുത്തില്ല. എന്നാൽ ഒരു ഊർജ്ജാവസ്ഥയിൽ നിന്ന് മറ്റൊന്നിലേക്ക് മാറുന്നതുവഴി ചില പ്രത്യേക അളവുകളിൽ ഇലക്ട്രോണുകൾക്ക് ഊർജ്ജം നേടുകയോ നഷ്ടപ്പെടുത്തുകയോ ചെയ്യാം. 1922-ൽ ബോർ ഭൗതികശാസ്ത്രത്തിനുള്ള നോബൽ സമ്മാനം നേടി[4].
ഊർജ്ജത്തിന് നിശ്ചിത വിലകളേ ഉണ്ടാവൂ എന്ന ബോർ പരികൽപന തെളിയിച്ച ഫ്രാങ്ക്-ഹേർട്സ് പരീക്ഷണം 1914-ലാണ് നടന്നത്. എന്നാൽ ഈ പരീക്ഷണം നടത്തുമ്പോൾ ഫ്രാങ്കും ഹേർട്സും ബോർ മാതൃകയെക്കുറിച്ച് അറിഞ്ഞിരുന്നില്ല[5]. ഇലക്ട്രോണുകളും മെർക്യുറി ആറ്റങ്ങളും തമ്മിൽ നടക്കുന്ന ഇലാസ്തികഘട്ടനങ്ങളും അനിലാസ്തികഘട്ടനങ്ങളും തമ്മിലുള്ള ഊർജ്ജ അതിർത്തി കണ്ടെത്തി അതിൽ നിന്ന് മെർക്യുറിയുടെ അയണീകരണ ഊർജ്ജം കണ്ടെത്തുകയായിരുന്നു അവരുടെ ഉദ്ദേശ്യം. ഈ സമയത്ത് ഇരുവരും ബെർളിൻ സർവ്വകലാശാലയിൽ ജോലി ചെയ്യുകയായിരുന്നു. സർവ്വകലാശാലയിൽ നിന്നുതന്നെയായിരുന്നു 1906-ൽ ഡോക്ടടറേറ്റും 1911-ൽ ഹാബിലിറ്റേഷനും ഫ്രാങ്ക് നേടിയത്. ഹേർട്സും അവിടെവച്ചുതന്നെ 1911-ൽ ഹെൻറിച്ച് റൂബൻസിന്റെ കീഴിൽ ഡോക്ടറേറ്റ് നേടിയ ശേഷം റൂബൻസിന്റെ സഹായിയായി പ്രവർത്തിക്കുകയായിരുന്നു.
പരീക്ഷണം[തിരുത്തുക]
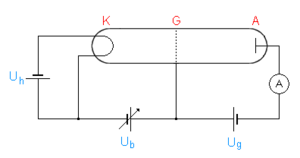
താഴ്ന്ന മർദ്ദത്തിലുള്ള മെർക്കുറി വാതകം നിറച്ച ഒരു ട്യൂബിലാണ് പരീക്ഷണം നടത്തിയത്[6][7]. വിദ്യുത് ഋണത കുറവാണ് എന്നതും തന്മാത്രയിൽ ഒരു ആറ്റം മാത്രമേ ഉള്ളൂ എന്നതും മെർക്കുറി വാതകം തിരഞ്ഞെടുക്കാൻ കാരണങ്ങളാണ്. ഈ ട്യൂബിൽ മൂന്ന് ഇലക്ട്രോഡുകൾ ഉണ്ടായിരുന്നു : ഇലക്ട്രോണുകളെ ഉത്സർജ്ജിക്കുന്ന കാതോഡ്, അവയുടെ പ്രവേഗം വർദ്ധിപ്പിക്കാൻ ഒരു ഗ്രിഡ്, ഒരു ആനോഡ്. ഒരു ഫിലമെന്റു് ചൂടാക്കുന്നത് വഴിയാണ് കാതോഡിൽ നിന്ന് ഇലക്ട്രോണുകളെ പുറപ്പെടുവിച്ചിരുന്നത്. ട്യൂബിലെ താപനില 110-115 ഡിഗ്രി സെൽഷ്യസായാണ് പരീക്ഷണത്തിൽ നിലനിർത്തിയിരുന്നത് (എന്നാൽ ആധുനികരീതിയിൽ ഇന്ന് ഈ പരീക്ഷണം നടത്തുമ്പോൾ ഉപയോഗിക്കുന്ന ഊഷ്മാവ് വ്യത്യസ്തമാണ്).
ആനോഡിലെ വോൾട്ടേജ് കാതോഡിലേതിനെക്കാൾ കൂടുതലാണെങ്കിലും ഗ്രിഡിലേതിനെക്കാൾ അല്പം കുറവായിരുന്നു. അതിനാൽ ഗ്രിഡ് കടക്കുമ്പോൾ അല്പമെങ്കിലും ഗതികോർജ്ജമുള്ള ഇലക്ട്രോണുകൾക്കു മാത്രമേ ആനോഡിലെത്താൻ സാധിക്കുമായിരുന്നുള്ളൂ[8]. കാതോഡും ഗ്രിഡും തമ്മിലുള്ള പൊടെൻഷ്യൽ വ്യത്യാസം ക്രമീകരിക്കാൻ മാർഗ്ഗമുണ്ടായിരുന്നു. ഈ പൊട്ടൻഷ്യൽ വ്യത്യാസവും വൈദ്യുതധാരയും അളക്കാൻ ഉപകരണങ്ങളും പരീക്ഷണവ്യവസ്ഥയുടെ ഭാഗമായുണ്ടായിരുന്നു.
ചിത്രത്തിൽ Uh ഫിലമെന്റ് ചൂടാക്കാനുപയോഗിക്കുന്ന വൈദ്യുതിയുടെ ഉറവിടമാണ്. സാധാരണ ഗതിയിൽ പ്രത്യാവർത്തിധാരാ വൈദ്യുതിയാണ് ഇതിന് ഉപയോഗിക്കുക. Ub കാതോഡും ഗ്രിഡും തമ്മിലുള്ള ക്രമീകരിക്കാവുന്ന പൊട്ടൻഷ്യൽ വ്യത്യാസവും Ug ഗ്രിഡും ആനോഡും തമ്മിലുള്ള നേരിയ ഋണവോൾട്ടേജുമാണ്. നേർധാരാ വൈദ്യുതി മാത്രമേ ഇവയ്ക്ക് ഉപയോഗിക്കാനാകൂ.
പരീക്ഷണഫലം[തിരുത്തുക]

ഈ പരീക്ഷണം നടത്തിയപ്പോൾ താഴെപ്പറയുന്ന കാര്യങ്ങളാണ് ഫ്രാങ്കിനും ഹേർട്സിനും കണ്ടെത്താൻ സാധിച്ചത്[6][7]:
- ഉൽകൃഷ്ടവാതകങ്ങളെപ്പോലെത്തന്നെ മെർക്കുറി വാതകത്തിലെ അണുക്കൾ തീരെ ഇലക്ട്രോൺ അഫിനിറ്റി കാണിച്ചില്ല
- താഴ്ന്ന പൊടെൻഷ്യൽ വ്യത്യാസങ്ങളിൽ (4.9 വോൾട്ട് വരെ) വോൾട്ടേജ് വർദ്ധിക്കുന്നതിനനുസരിച്ച് വൈദ്യുതധാരയും വർദ്ധിച്ചു. അതായത്, പൊടെൻഷ്യൽ വ്യത്യാസം വർദ്ധിച്ചതോടെ ട്യൂബിലെ വൈദ്യുതമണ്ഡലം വർദ്ധിക്കുകയും പ്രതീക്ഷിച്ചതുപോലെ ഇലക്ട്രോണുകൾ കൂടുതൽ വേഗത്തോടെ ഗ്രിഡ് കടക്കുകയും ആനോഡിലെത്തുകയും ചെയ്തു
- പൊടെൻഷ്യൽ വ്യത്യാസം 4.9 വോൾട്ട് ആയപ്പോൾ വൈദ്യുതധാര ഗണ്യമായി കുറഞ്ഞു
- ഇതിനുശേഷം വോൾട്ടേജ് വർദ്ധിക്കുന്നതിനനുസരിച്ച് വൈദ്യുതധാര വർദ്ധിച്ചു. പൊടെൻഷ്യൽ വ്യത്യാസം 9.8 വോൾട്ട് (4.9 -ന്റെ ഇരട്ടി) ആയപ്പോൾ വീണ്ടും ഗണ്യമായി കുറഞ്ഞു
- 4.9 വോൾട്ടിന്റെ ഇടവേളകളിൽ വൈദ്യുതധാര പൊടുന്നനെ ഗണ്യമായി കുറയുന്ന ഈ പ്രതിഭാസം 100 വോൾട്ടോളം വരെ തുടർന്നു
വിശദീകരണം[തിരുത്തുക]

ഇലാസ്തികവും അനിലാസ്തികവുമായ ഘട്ടനങ്ങൾ (Elastic and Inelastic Collisions) ഉപയോഗിച്ച് ഈ പരീക്ഷണഫലങ്ങളെ വിശദീകരിക്കാം[5]. ഇലാസ്തികഘട്ടനത്തിൽ പങ്കെടുക്കുന്ന വസ്തുക്കളുടെ മൊത്തം ഗതിഗോർജ്ജം ഘട്ടനത്തിനുമുമ്പും ശേഷവും തുല്യമായിരിക്കും. എന്നാൽ അനിലാസ്തികഘട്ടനങ്ങളിൽ ഗതികോർജ്ജത്തിന്റെ ഒരു ഭാഗം മറ്റേതെങ്കിലും രൂപത്തിലെ ഊർജ്ജമായി മാറാം.
താഴ്ന്ന പൊടെൻഷ്യൽ വ്യത്യാസങ്ങളിൽ ഇലക്ട്രോണുകൾക്ക് വളരെക്കുറവ് ഗതികോർജ്ജം മാത്രമേ കൈവരിക്കാനായുള്ളൂ. ട്യൂബിലെ മെർക്കുറി ആറ്റങ്ങളുമായുള്ള ഇവയുടെ ഘട്ടനങ്ങൾ പൂർണ്ണമായും ഇലാസ്തികമായിരുന്നു. കാരണം, ബോർ മാതൃകയിലെ താഴ്ന്ന ഊർജ്ജസ്ഥിതിയിൽ നിന്ന് ഉയർന്നതിലേക്ക് ആറ്റത്തിലെ ഇലക്ട്രോണിനെ ഉയർത്താൻ പര്യാപ്തമായ ഊർജ്ജം ട്യൂബിലെ ഇലക്ട്രോണുകൾക്ക് ഉണ്ടാകുന്നതുവരെ അവയിൽ നിന്ന് അനിലാസ്തികഘട്ടനങ്ങളിലൂടെ ആറ്റത്തിന് ഗതികോർജ്ജമാല്ലാതെ ഊർജ്ജം സ്വീകരിക്കാനാകില്ല.ഇലാസ്തികഘട്ടനങ്ങൾ നടക്കുമ്പോൾ ട്യൂബിലെ മൊത്തം ഗതികോർജ്ജം സ്ഥിരമായിരിക്കുന്നു. മെർക്കുറി ആറ്റങ്ങളുമായി താരതമ്യം ചെയ്യുമ്പോൾ ഇലക്ട്രോണുകളുടെ പിണ്ഡം വളരെക്കുറവാണ് (ഏകദേശം നാല് ലക്ഷത്തിൽ ഒരു ഭാഗം മാത്രം) എന്നതിനാൽ ഈ ഗതികോർജ്ജത്തിന്റെ സിംഹഭാഗവും ഇലക്ട്രോണുകളുടെ പക്കലാണുണ്ടാവുക. ഉയർന്ന പൊടെൻഷ്യൽ വ്യത്യാസം കൂടുതൽ ഇലക്ട്രോണുകളെ ഗ്രിഡ് കടന്ന് ആനോഡിലെത്താൻ സഹായിക്കുന്നു. അങ്ങനെ വൈദ്യുതധാര വർദ്ധിക്കുന്നു. പൊടെൻഷ്യൽ വ്യത്യാസം 4.9 വോൾട്ട് ആകുന്നതുവരെ ഇതാണ് സംഭവിക്കുന്നത്.
ഒരു മെർക്കുറി ആറ്റത്തിന് അനിലാസ്തികഘട്ടനത്തിൽ സ്വീകരിക്കുവാനാവുന്ന ഏറ്റവും ചെറിയ ഊർജ്ജം 4.9 ഇലക്ട്രോൺ വോൾട്ടാണ്. പൊടെൻഷ്യൽ വ്യത്യാസം 4.9 വോൾട്ടാകുമ്പോൾ ഗ്രിഡിലെത്തുന്ന ഓരോ ഇലക്ട്രോണിന്റെയും കൈവശം കൃത്യം ഇത്ര ഗതികോർജ്ജമുണ്ടായിരിക്കും. അതിനാൽ മെർക്കുറി ആറ്റവും ഇലക്ട്രോണും തമ്മിലുള്ള ഘട്ടനം അനിലാസ്തികമാകാൻ ഏറെ സാധ്യതയുണ്ട്. ഇത് സംഭവിക്കുമ്പോൾ ഇലക്ട്രോണിന്റെ 4.9 ഇലക്ട്രോൺ വോൾട്ട് ഊർജ്ജം നഷ്ടപ്പെടുകയും മെർക്കുറി ആറ്റത്തിലെ ഒരു ഇലക്ട്രോൺ ഉയർന്ന ഊർജ്ജസ്ഥിതിയിലേക്ക് മാറുകയും ചെയ്യുന്നു. ഇങ്ങനെ ഗതികോർജ്ജം ഏറെക്കുറെ പൂർണ്ണമായി നഷ്ടപ്പെട്ട ഇലക്ട്രോണിന് ഗ്രിഡും ആനോഡും തമ്മിലുള്ള നേരിയ ഋണവോൾട്ടേജ് മറികടക്കാനാകാതെ വരികയും വൈദ്യുതധാര ഗണ്യമായി കുറയുകയും ചെയ്യുന്നു.
പൊടെൻഷ്യൽ വ്യത്യാസം 4.9 വോൾട്ടിനെക്കാൾ വർദ്ധിക്കുമ്പോൾ ഒരു അനിലാസ്തികഘട്ടനം വഴി ഇലക്ട്രോണിന്റെ ഗതികോർജ്ജത്തിൽ നിന്ന് 4.9 ഇലക്ട്രോൺ വോൾട്ട് കുറയുന്നു. എന്നാൽ ഇതിനു ശേഷവും ഇലക്ട്രോണിന് ഗതികോർജ്ജം ബാക്കിയുണ്ടാവും. ഇതുപയോഗിച്ച് ഇലക്ട്രോൺ ഗ്രിഡിൽ നിന്ന് ആനോഡിലേക്കെത്തുകയും വൈദ്യുതധാര വർദ്ധിക്കുകയും ചെയ്യുന്നു. ഇതിന് ഭംഗം സംഭവിക്കുക ഒരു ഇലക്ട്രോൺ രണ്ടു തവണ അനിലാസ്തികഘട്ടനത്തിൽ ഏർപ്പെടുമ്പോളാണ്. കാതോഡും ഗ്രിഡും തമ്മിലുള്ള പൊടെൻഷ്യൽ വ്യത്യാസം 9.8 ആകുമ്പോളാണ് ഇക്കാര്യം നടക്കുക. അതായത്, പൊടെൻഷ്യൽ വ്യത്യാസം 9.8 വോൾട്ടാകുമ്പോൾ വൈദ്യുതധാര വീണ്ടും ഗണ്യമായി കുറയുന്നു.
വൈദ്യുതധാര മെല്ലെ വർദ്ധിക്കുകയും പൊടുന്നനെ ഗണ്യമായി കുറയുകയും ചെയ്യുന്ന ഈ പ്രതിഭാസം 4.9 വോൾട്ടിന്റെ ഇടവേളകളിൽ തുടരുന്നു
വിശദീകരണത്തിലെ തെറ്റ്[തിരുത്തുക]

4.9 ഇലക്ട്രോൺ വോൾട്ട് മെർക്കുറി ആറ്റത്തെ അയണീകരിക്കാൻ വേണ്ട ഊർജ്ജമാണെന്നാണ് ഫ്രാങ്കും ഹേർട്സും കരുതിയിരുന്നത്[9]. തങ്ങളുടെ പരീക്ഷണഫലങ്ങൾ പ്രസിദ്ധീകരണത്തിൽ വിശദീകരിച്ചിടത്ത് അവർ നൽകിയതും ഇങ്ങനെത്തന്നെ. 1916 വരെ ഈ വിശ്വാസത്തിൽ അവർ തുടർന്നു[10]. യഥാർത്ഥത്തിൽ മെർക്കുറി ആറ്റത്തിലെ ഇലക്ട്രോണിനെ n=1 എന്ന ഊർജ്ജസ്ഥിതിയിൽ നിന്ന് (ground state) n=2 എന്ന ഊർജ്ജസ്ഥിതിയിലേക്ക് (first excited state) ഉയർത്താനാവശ്യമായ ഊർജ്ജമാണ് 4.9 ഇലക്ട്രോൺ വോൾട്ട്.
അയണീകരണ ഉർജ്ജമാണ് 4.9 ഇലക്ട്രോൺ വോൾട്ട് എന്നുണ്ടെങ്കിൽ തന്റെ സിദ്ധാന്തം തെറ്റാണെന്നു വരുമെന്ന് മനസ്സിലാക്കിയ ബോർ തന്നെ ഈ വിശദീകരണത്തെക്കുറിച്ച് കൂടുതൽ പഠിക്കാൻ ശ്രമിച്ചു. അയണീകൃതമല്ലാത്ത മെർക്കുറി ആറ്റത്തിന്റെ രണ്ട് ഊർജ്ജസ്ഥിതികൾ തമ്മിലുള്ള വ്യത്യാസം തന്നെയാകാം ഇത് എന്നും അങ്ങനെയെങ്കിൽ പരീക്ഷണഫലങ്ങൾ തന്റെ സിദ്ധാന്തങ്ങളുമായി ഒത്തു പോകുമെന്നും അദ്ദേഹം വിശ്വസിച്ചു. കാണാനാകാത്ത ഫോട്ടോൺ ഉത്സർജ്ജിക്കപ്പെട്ടതു മൂലം ഇലക്ട്രോഡുകളിലുണ്ടായ ഫോട്ടോ ഇലക്ട്രിക് പ്രഭാവമാകാം വൈദ്യുതധാര വർദ്ധിച്ചതിനും അയണികരണ ഊർജ്ജമായി ഫ്രാങ്കും ഹേർട്സും ഇതിനെ വിലയിരുത്തിയതിനും കാരണം എന്ന് ബോർ പരികൽപന നടത്തി. റുഥർഫോർഡുമായി കൂടിയാലോചിച്ച ശേഷം ഇത് സ്ഥിരീകരിക്കാൻ ഒരു പരീക്ഷണം നടത്താൻ അദ്ദേഹം ശ്രമിച്ചുവെങ്കിലും ഒരു തീപിടിത്തത്തിന്റെ ഫലമായി പരീക്ഷണോപകരണം ഉപയോഗശൂന്യമായതിനാൽ ഇതിന് സാധിച്ചില്ല[9].
ബോർ സിദ്ധാന്തത്തെക്കുറിച്ച് അറിഞ്ഞിരുന്ന മറ്റു ശാസ്ത്രജ്ഞർ പിന്നീട് പ്രസിദ്ധീകരണം വായിച്ച് അത് ബോർ സിദ്ധാന്തത്തെ ശരിവയ്ക്കുന്നു എന്ന് മനസ്സിലാക്കി. പരീക്ഷണങ്ങളിലൂടെ കൂടുതൽ തെളിവുകൾ നൽകുകയും ചെയ്തു[5].
ഫോട്ടോൺ ഉത്സർജ്ജനം[തിരുത്തുക]
മെർക്കുറി വാതകമുപയോഗിച്ചുള്ള ഫ്രാങ്ക്-ഹേർട്സ് പരീക്ഷണത്തിന്റെ ഭാഗമായി 2537 ആങ്സ്ട്രോം[11] തരംഗദൈർഘ്യമുള്ള ഫോട്ടോൺ ഉത്സർജ്ജിക്കപ്പെടുന്നുണ്ട്. നേരത്തെ ഇലക്ട്രോണുകളുമായി കൂട്ടിയിടിച്ചതിന്റെ ഫലമായി ഉയർന്ന ഊർജ്ജാവസ്ഥയിലെത്തിയ മെർക്യുറി ആറ്റങ്ങൾ വികിരണത്തിലൂടെ ഊർജ്ജം നഷ്ടപ്പെട്ട് പഴയ അവസ്ഥയിലേക്കുതന്നെ തിരിച്ചുപോവുമ്പോഴാണ് ഇത് സംഭവിക്കുന്നത്. വിദ്യുത്കാന്തിക വർണ്ണരാജിയുടെ അൾട്രാവയലറ്റ് ഭാഗത്താണ് ഈ തരംഗദൈർഘ്യം. നഗ്നനേത്രങ്ങളല്ലാതെ പ്രകാശം തിരിച്ചറിയാൻ മറ്റ് ഉപകരണങ്ങളൊന്നുമില്ലാത്തിനാൽ പരീക്ഷണത്തിനിടയിൽ ഫ്രാങ്കും ഹേർട്സും ഇത് ദർശിച്ചില്ല[12]. എന്നാൽ പിന്നീട് 1924-ൽ ഹേർട്സ് നടത്തിയ പരിഷ്കൃതമായ പരീക്ഷണത്തിൽ ഈ ഫോട്ടോണിന്റെ സാന്നിദ്ധ്യമറിയാൻ സാധിച്ചു[13]. 2537 ആങ്സ്ട്രോം തരംഗദൈർഘ്യമുള്ള ഫോട്ടോണിന്റെ ഊർജ്ജം 4.9 ഇലക്ട്രോൺ വോൾട്ടാണെന്നുള്ളത് പരീക്ഷണഫലത്തിന്റെ വിശദീകരണത്തിന് കൂടുതൽ ഉറപ്പ് നൽകുന്നു.
അയണീകരണം[തിരുത്തുക]
ഉയർന്ന പൊട്ടൻഷ്യൽ വ്യത്യാസങ്ങളിൽ പരീക്ഷണം നടത്തുമ്പോൾ ഇലക്ട്രോണുമായുള്ള ഘട്ടനത്തിന്റെ ഫലമായി മെർക്കുറി ആറ്റം അയണീകൃതമാകാൻ സാധ്യതയുണ്ട്. ഇങ്ങനെ വരുമ്പോൾ സ്വതന്ത്രമാക്കപ്പെടുന്ന ഉയർന്ന ഊർജ്ജമുള്ള ഇലക്ട്രോൺ വൈദ്യുതമണ്ഡലത്തിൽ നിന്ന് വീണ്ടും ഊർജ്ജം നേടുകയും ഘട്ടനങ്ങളിലൂടെ കൂടുതൽ മെർക്കുറി ആറ്റങ്ങളെ അയണീകരിക്കുകയും ചെയ്യുന്നു. ഈ ചെയിൻ റിയാക്ഷൻ ട്യൂബിലെ മെർക്കുറി വാതകം ചാലകതയുള്ള പ്ലാസ്മയായി മാറുന്നതിലാണ് കലാശിക്കുക. ഇങ്ങനെ വരുമ്പോൾ ട്യൂബിലെ വാതകം നീലനിറത്തിൽ തിളങ്ങുകയും വൈദ്യുതധാര ഗണ്യമായി വർദ്ധിക്കുകയും ചെയ്യുന്നു. പ്ലാസ്മ രൂപവത്കരണം നടക്കുന്ന പൊടെൻഷ്യൽ വ്യത്യാസം ട്യൂബിന്റെ ഘടന, വാതകത്തിന്റെ മർദ്ദം, താപനില മുതലായ ഘടകങ്ങളെ ആശ്രയിച്ചിരിക്കുന്നു. അയണീകരണം നടന്നുകഴിഞ്ഞാൽ പിന്നെ വോൾട്ടേജ് കുറയ്ക്കാതെ പരീക്ഷണം തുടരാനാകില്ല.
മറ്റ് വാതകങ്ങളിൽ[തിരുത്തുക]
മെർക്കുറി വാതകത്തിനു പകരം നിയോൺ ഉപയോഗിച്ചാലും ഈ പ്രഭാവം കാണാൻ സാധിക്കും[6]. 4.9 വോൾട്ടിനു പകരം 19 വോൾട്ടിന്റെ ഇടവേളകളിലാണ് നിയോൺ ഉപയോഗിച്ചാൽ വൈദ്യുതധാരയിലെ പൊടുന്നനെയുള്ള കുറവ് കാണാൻ സാധിക്കുക. ഓരോ അനിലാസ്തികഘട്ടനത്തിലും 18.3-19.5 ഇലക്ട്രോൺ വോൾട്ട് ഊർജ്ജം സ്വീകരിക്കുന്ന നിയോൺ ഇലക്ട്രോൺ അതിനുശേഷം 16.57-16.79 ഇലക്ട്രോൺ വോൾട്ട് ഊർജ്ജസ്ഥിതിയിലേക്ക് മാറുന്നു. ഈ മാറ്റം നടക്കുന്നത് ഓറഞ്ച് നിറത്തിലുള്ള ഫോട്ടോൺ ഉത്സർജ്ജിക്കുന്നതു വഴിയാണ്. അതിനാൽ നിയോൺ ഉപയോഗിച്ചുള്ള ഫ്രാങ്ക്-ഹേർട്സ് പരീക്ഷണം നടത്തുന്ന ട്യൂബിൽ ഓറഞ്ച് നിറത്തിലുള്ള ബാൻഡുകൾ കാണപ്പെടുന്നു.
ഹീലിയം, ആർഗൺ, ക്രിപ്റ്റോൺ മുതലായ അലസവാതകങ്ങളും ഈ പരീക്ഷണത്തിന് ഉപയോഗിക്കാവുന്നതാണ്. ഫ്രാങ്കും ഹേർട്സും തന്നെ ഹീലിയം വാതകമുപയോഗിച്ചുള്ള പരീക്ഷണവും നടത്തിയിരുന്നു.
1925-ലെ നോബൽ സമ്മാനം[തിരുത്തുക]
ഫ്രാങ്കും ഹേർട്സും 1925-ലെ ഭൗതികശാസ്ത്രത്തിനുള്ള നോബൽ സമ്മാനം പങ്കിട്ടു. നീൽസ് ബോർ തന്റെ ആറ്റം മാതൃകയുടെ പേരിൽ 1922-ൽ തന്നെ നോബൽ നേടിയിരുന്നു. ഇലക്ട്രോണുകളും ആറ്റങ്ങളും തമ്മിലുള്ള ഘട്ടനങ്ങളെ സംബന്ധിക്കുന്ന നിയമങ്ങൾ കണ്ടെത്തിയതിനാണ് അവർ സമ്മാനിതരായത്[1]. പുരസ്കാരദാനപ്രസംഗം ഈ പ്രസ്താവനയോടെയാണ് അവസാനിച്ചത്[14]:
| “ | പ്രൊഫസർ ഫ്രാങ്ക്, പ്രൊഫസർ ഹേർട്സ്. നിരവധി പരികൽപനകളുടെ പ്രളയത്തിന് വിധേയമായിക്കൊണ്ടിരിക്കുന്ന ഒരു വിഷയത്തിൽ തെളിഞ്ഞ ചിന്തയിലൂടെയും കഠിനതകൾ നിറഞ്ഞ പരീക്ഷണങ്ങളിലൂടെയും ഭാവി ഗവേഷണങ്ങൾക്ക് നിങ്ങൾ ഉറച്ച അടിത്തറ നൽകിയിരിക്കുന്നു. നിങ്ങളുടെ പ്രവർത്തനങ്ങൾക്ക് നന്ദിസൂചകമായി, അഭ്യുദയകാംക്ഷയോടെ, ഞങ്ങളുടെ രാജാവിൽ നിന്ന് 1925-ലെ ഭൗതികശാസ്ത്രത്തിനുള്ള നോബൽ സമ്മാനം ഏറ്റുവാങ്ങാൻ ഞാൻ അഭ്യർത്ഥിക്കുന്നു. | ” |
ജൂതനായതിനാൽ പിന്നീട് ഹിറ്റ്ലറുടെ ഭരണകാലത്ത് ജർമ്മനി വിടേണ്ടിവന്ന ഫ്രാങ്ക് ജർമ്മൻകാർ നോബൽ പുരസ്കാരത്തിലെ മെഡൽ കണ്ടുകെട്ടാതിരിക്കാൻ കോപ്പൺഹാഗനിലെ സൈദ്ധാന്തികഭൗതികശാസ്ത്രത്തിനുള്ള ബോർ ഇന്സ്റ്റിറ്റ്യൂട്ടിൽ സൂക്ഷിക്കാനേൽപിച്ചു. മറ്റൊരു നോബൽ ജേതാവായ മാക്സ് ലോയും ഇതുതന്നെ ചെയ്തിരുന്നു. 1940 ഏപ്രിലിൽ ജർമ്മൻ സൈന്യം ഡെൻമാർക്ക് കീഴടക്കിയപ്പോൾ മെഡലുകൾ രക്ഷിക്കാൻ ബോർ വഴികളാലോചിച്ചു. ഒടുവിൽ അവിടെത്തന്നെ ജോലിചെയ്തിരുന്ന രസതന്ത്രനോബൽ ജേതാവായ ജോർജ്ജ് ദി ഹെവെസി മെഡലുകളിലെ സ്വർണം അക്വാ റീജിയയിൽ ലയിപ്പിച്ചാണ് ജർമ്മൻ പട്ടാളത്തിൽ നിന്ന് രക്ഷിച്ചെടുത്തത്. യുദ്ധാനന്തരം ലായനിയിൽ നിന്ന് സ്വർണ്ണം വേർതിരിച്ചെടുക്കുകയും റോയൽ സ്വീഡിഷ് അക്കാഡമിക്ക് നൽകുകയും ചെയ്തു. ഇതിൽ നിന്ന് പുനർനിർമ്മിക്കപ്പെട്ട മെഡൽ 1952 ജനുവരി 31-ന് ചിക്കാഗോ സർവ്വകലാശാലയിലെ ചടങ്ങിൽ വച്ച് ഫ്രാങ്കിന് വീണ്ടും സമ്മാനിച്ചു[15].
അവലംബം[തിരുത്തുക]
- ↑ 1.0 1.1 The Nobel Prize in Physics 1925
- ↑ USEPA : Rutherford-Bohr Model
- ↑ "The Bohr Model of Atoms". Archived from the original on 2009-04-17. Retrieved 2009-07-28.
- ↑ The Nobel Prize in Physics 1922
- ↑ 5.0 5.1 5.2 The Franck-Hertz experiment supports Bohr's model
- ↑ 6.0 6.1 6.2 HyperPhysics : The Franck-Hertz Experiment
- ↑ 7.0 7.1 Physics LAB : Famous Discoveries: The Franck-Hertz Experiment
- ↑ "WebPhysics : PHYSICS 320 LAB : THE FRANCK-HERTZ EXPERIMENT". Archived from the original on 2009-04-19. Retrieved 2009-07-28.
- ↑ 9.0 9.1 Men who made a new physics: physicists and the quantum theory By Barbara Lovett Cline
- ↑ Twentieth Century Physics By Laurie M. Brown, Abraham Pais, A. B. Pippard
- ↑ Quantum mechanics: an introduction By Walter Greiner
- ↑ Fundamentals of light sources and lasers By Mark Csele
- ↑ Nonrelativistic quantum mechanics By Anton Z. Capri
- ↑ The Nobel Prize in Physics 1925 : Presentation Speech
- ↑ "The Nobel Prize Medals and the Medal for the Prize in Economics". Archived from the original on 2007-10-27. Retrieved 2009-08-28.
പുറത്തേക്കുള്ള കണ്ണികൾ[തിരുത്തുക]
- ഫ്രാങ്ക്-ഹേർട്സ് പരീക്ഷണം : സിമുലേഷൻ Archived 2009-02-10 at the Wayback Machine.
- ഫ്രാങ്ക്-ഹേർട്സ് പരീക്ഷണം : പുതിയ കണ്ടെത്തലുകൾ Archived 2009-01-08 at the Wayback Machine.
- ഫ്രാങ്ക്-ഹേർട്സ് പരീക്ഷണം : ലിങ്കുകളുടെ സമാഹാരം




